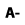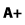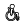Puede realizar búsquedas exactas dentro de este documento, ingrese el texto a buscar en la siguiente casilla:


RESOLUCIÓN 810 DE 2021
(junio 16)
Diario Oficial No. 51.707 de 16 de junio de 2021
<Rige a partir del 14 de junio de 2023>
MINISTERIO DE SALUD Y PROTECCIÓN SOCIAL
Por la cual se establece el reglamento técnico sobre los requisitos de etiquetado nutricional y frontal que deben cumplir los alimentos envasados o empacados para consumo humano.
EL MINISTRO DE SALUD Y PROTECCIÓN SOCIAL,
en ejercicio de sus atribuciones legales, especialmente de las conferidas por los artículos 267 de la Ley 09 de 1979, 10 de la Ley 1355 de 2009, y 2 numerales 4, 7 y 30 del Decreto-ley 4107 de 2011, y
CONSIDERANDO:
Que el artículo 78 de la Constitución Política dispone que “(…) Serán responsables, de acuerdo con la ley, quienes en la producción y en la comercialización de bienes y servicios, atenten contra la salud, la seguridad y el adecuado aprovechamiento a consumidores y usuarios”.
Que el acuerdo sobre Obstáculos Técnicos al Comercio (OTC) de la Organización Mundial del Comercio, al cual adhirió Colombia a través de la Ley 170 de 1994, así como la Decisión 419 de la Comisión de la Comunidad Andina (CAN), establecen que los países tienen derecho a adoptar las medidas necesarias para asegurar la calidad de sus exportaciones, o para la protección de la salud y la vida de las personas, para la protección del medio ambiente, o para la prevención de prácticas que pueden inducir a error, para lo cual, según lo allí establecido, pueden adoptar reglamentos técnicos que incluyan prescripciones en materia de terminología, símbolos, embalaje, marcado o etiquetado, aplicables a productos.
Que la Decisión 562 de la Comisión de la Comunidad Andina (CAN) contempla las directrices para la elaboración, adopción y aplicación de reglamentos técnicos en los países miembros de la Comunidad Andina y en el nivel comunitario, estableciendo en el artículo 4o que el reglamento técnico “es un documento adoptado para hacer frente a problemas o amenazas de problemas que pudieran afectar la seguridad, sanidad, protección del medio ambiente o seguridad nacional”; y la Decisión 506 de 2001 expedida por la CAN decidió sobre el reconocimiento y aceptación de certificados de productos a ser comercializados en la Comunidad Andina.
Que de conformidad con lo establecido en el artículo 28 de la Decisión Andina 850 de 2019, los reglamentos técnicos se establecen para garantizar, entre otros, los siguientes objetivos legítimos: los imperativos de la seguridad nacional, la protección de la salud o seguridad humana, de la vida, la salud animal o vegetal, el medio ambiente y la prevención de prácticas que puedan inducir a error a los consumidores.
Que la Ley 1480 de 2011 expide el Estatuto del Consumidor y dicta otras disposiciones, en la cual se define como productor “Quien, de manera habitual, directa o indirecta, diseñe, produzca, fabrique, ensamble o importe productos. También se reputa productor, quien diseñe, produzca, fabrique, ensamble, o importe productos sujetos a reglamento técnico o medida sanitaria y fitosanitaria” y además se señala en el artículo 6o sobre calidad, idoneidad y seguridad de los productos que “Todo productor debe asegurar la idoneidad y seguridad de los bienes y servicios que ofrezca o ponga en el mercado, así como la calidad ofrecida. En ningún caso estas podrán ser inferiores o contravenir lo previsto en reglamentos técnicos y medidas sanitarias o fitosanitarias”.
Que el Decreto número 1074 de 2015, Único Reglamentario del Sector Comercio, Industria y Turismo define los lineamientos técnicos para adoptar buenas prácticas de reglamentación técnica y en el Capítulo VII, Sección 5 del Capítulo 7 del Título 1 de la Parte 2 del Libro 2 dictan normas relativas al Subsistema Nacional de la Calidad, con énfasis en los procedimientos de reglamentación necesarios para la expedición de las normas nacionales.
Que las directrices para la elaboración, adopción y aplicación de reglamentos técnicos en los Países Miembros de la Comunidad Andina y a nivel comunitario se encuentran contenidas en la Decisión 827 de 2018 de la Comunidad Andina y el procedimiento administrativo para la elaboración, adopción y aplicación de reglamentos técnicos, medidas sanitarias y fitosanitarias en el ámbito agroalimentario, en el artículo 2.13.2.1.1. y s.s. del Decreto número 1071 de 2015, que se ha observado en la elaboración del presente reglamento técnico.
Que de acuerdo con el estudio “Estimación de la carga global de enfermedad en Colombia 2017: nuevos aspectos metodológicos” realizado por el Instituto de Evaluación y Medición de la Universidad de Washington para Colombia, el exceso de peso se relaciona con graves complicaciones de salud y de años de vida saludables perdidos (AVISAS). El Índice de Masa Corporal alto (exceso de peso), tiene un mayor riesgo atribuible con la enfermedad cardiovascular (3,15%), y con enfermedades endocrinas (2,32%), así mismo, la hipertensión juega un papel fundamental en la enfermedad cardiovascular (6,68%) y los factores dietarios que contribuyen con el 5,96% de riesgo atribuible para enfermedad cardiovascular.
Que según el estudio sobre los efectos sobre la salud de los riesgos alimentarios en 195 países, 1990-2017: Estudio Global de la Carga de Enfermedades 2017, y publicado en el año 2019, a nivel mundial los factores dietarios y el consumo elevado de sodio, bebidas azucaradas y ácidos grasos trans tiene una relación directa con las muertes por enfermedades cardiovasculares, cáncer y diabetes.
Que de acuerdo con las estadísticas vitales del Departamento Administrativo Nacional de Estadística del año 2018, en el país las enfermedades cardiovasculares se encuentran dentro de las diez primeras causas de mortalidad y ocasionaron el 27,6% del total de fallecimientos. Entre los principales factores de riesgo de enfermedad cardiovascular se encuentran la hipertensión arterial y la hipercolesterolemia; según la Encuesta Nacional de Salud de 2007, el 22,82% de la población de 18 a 69 años presentó cifras de presión arterial elevadas y el 7.82% presentó hipercolesterolemia (colesterol total por encima de 240 mg/ dl). Se estima que aproximadamente el 62% de los casos de hipertensión se relacionan con la ingesta excesiva de sal en la alimentación; mientras que la hipercolesterolemia, se relaciona con la ingesta excesiva de grasas saturadas y trans, y constituye por su prevalencia el segundo factor de riesgo para enfermedad cardiovascular.
Que la última Encuesta de Situación Alimentaria y Nutricional en Colombia (ENSIN) (2015), arrojó resultados relevantes en cuanto a la alta prevalencia de consumo de alimentos procesados en todos los grupos de edad, por encima del 50% de la población, e incluso llegando hasta el 91.4% y el aumento en cuanto a la prevalencia de sobrepeso y obesidad, especialmente en los escolares, en quienes se incrementó de 18,8% en 2010 a 24,4% en 2015. Asimismo, uno de cada tres jóvenes y adultos tiene sobrepeso (37,7%), mientras que uno de cada cinco es obeso (18,7%). En este sentido, el 56,4% de la población presenta exceso de peso, lo que significa un incremento de 5,2 puntos porcentuales con respecto al 2010. Además, más de la mitad de las mujeres adultas, 59,6%, y el 39,3% de los hombres presentan obesidad abdominal, situación que favorece el desarrollo de enfermedades cardiovasculares e insulinorresistencia.
Que la Organización Mundial de la Salud (OMS) y el World Cancer Research Fund (WCRF) coinciden en que los factores más importantes que promueven el aumento de peso y la obesidad, así como las enfermedades no transmisibles (ENT), son el aumento en el consumo de productos de bajo valor nutricional y alto contenido en azúcares adicionados, grasas y sal, tales como los snacks y la comida rápida, la ingesta habitual de bebidas azucaradas, y la disminución en la actividad física.
Que la Organización Mundial de la Salud (OMS) recomienda en el Informe para acabar con la obesidad infantil del año 2016 “poner en marcha un etiquetado del frente del envase fácil de interpretar, apoyado en la educación del público para que tanto los adultos como los niños tengan conocimientos básicos en materia de nutrición”.
Que la Organización Panamericana de la Salud (OPS), en la línea estratégica 3 del Plan de acción para la prevención de la obesidad en la niñez y la adolescencia. (2014-2019), insta a los gobiernos a “elaborar y establecer normas para el etiquetado del frente del envase que promuevan las elecciones saludables al permitir identificar los alimentos de alto contenido calórico y bajo valor nutricional de manera rápida y sencilla”, igualmente, este organismo en su informe: “El etiquetado frontal como instrumento de política para prevenir enfermedades no transmisibles en la Región de las Américas de 2020”, afirma que para ayudar a la población de la Región a cumplir con las recomendaciones de la Organización Mundial de la Salud (OMS) y protegerla contra los principales factores de riesgo que perjudican su salud y desarrollo, el objetivo regulatorio del etiquetado frontal debe ser que: “los consumidores puedan identificar correcta, rápida y fácilmente los productos que contienen cantidades excesivas de nutrientes críticos de preocupación para la salud pública (que incluyen los azúcares, grasas saturadas, grasas trans y sodio), pues su ingesta inadecuada y/o excesiva es resultado, en gran medida, de la amplia disponibilidad, asequibilidad y promoción de productos alimentarios procesados y ultraprocesados que contienen cantidades excesivas de los mismos”.
Que de acuerdo con lo señalado en el artículo 3o. Derechos y deberes de los consumidores y usuarios, de la Ley 1480 de 2011, el consumidor tiene 1. Derechos: (…) 1.3. Derecho a recibir información: Obtener información completa, veraz, transparente, oportuna, verificable, comprensible, precisa e idónea respecto de los productos que se ofrezcan o se pongan en circulación, así como sobre los riesgos que puedan derivarse de su consumo o utilización, los mecanismos de protección de sus derechos y las formas de ejercerlos.
Que según la Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO) en el documento “Influir en los entornos alimentarios en pro de dietas saludables - 2016”, afirma que deben cambiarse las etiquetas a fin de que: 1) sean fáciles de entender, 2) no requieran conocimientos previos sobre nutrición, y 3) los consumidores puedan encontrarlas fácilmente en el envase, con el objetivo de que el entorno alimentario sea saludable y que garantice que haya alimentos saludables y nutritivos disponibles, asequibles, aceptables y deseables para todas las personas.
Que de acuerdo con la Declaración del Relator Especial de las Naciones Unidas sobre el derecho a la salud en 2020, se instó a los Estados a abordar el impacto mundial de las enfermedades no transmisibles, adoptando políticas de etiquetado frontal como advertencia de los alimentos y bebidas que contienen cantidades excesivas de nutrientes críticos, reconociéndola como una medida regulatoria adecuada, que contribuye a las obligaciones del Estado en materia de derechos humanos y que permita a los consumidores a tomar decisiones informadas sobre sus dietas, sin realizar esfuerzos adicionales ni requerir conocimientos cualificados.
Que de acuerdo a los resultados del análisis de impacto normativo, con proyecciones a 25 años, el costo de la implementación de este acto administrativo, sería de 697.758 millones de pesos (COP), el cual implica, estudios de consumidores, nuevas etiquetas, diseños de productos, acciones de Inspección, Vigilancia y Control, procesos de evaluación de conformidad. Mientras que los ahorros en salud, establecidos como beneficios, se estiman en 2.787.180 millones de pesos (COP), lo cual implica una mitigación de las prevalencias de exceso de peso y de su contribución con las enfermedades no transmisibles y el costo asociado a ello, como costos directos e indirectos en salud, gastos de bolsillo, disminución de muertes prematuras y por ende, mejoramiento de la productividad en el país. De tal manera, que esta medida resulta con una relación de costo-beneficio de 3.99, indicando que es la mejor alternativa en comparación con campañas informativas y el statu quo.
Que la información nutricional que contengan los empaques de los alimentos es un elemento de apoyo a las políticas de alimentación del país, y, por lo tanto, se hace necesario establecer con el presente reglamento técnico los requisitos en materia de etiquetado nutricional y frontal como medida de protección al consumidor, para presentar una información clara y comprensible en la etiqueta.
Que, en cumplimiento de los Decretos números 210 de 2003, 1471 de 2014, 1595 de 2015 y 1468 de 2020, este Ministerio solicitó concepto previo al Ministerio de Comercio, Industria y Turismo, rendido a través de la Dirección de Regulación mediante 2-2021- 003113 en el sentido de que el proyecto de resolución en principio no restringirá el comercio más de lo necesario para alcanzar el objetivo legítimo ahí mencionado.
Que el reglamento técnico que se adopta mediante la presente resolución fue notificado a la Organización Mundial del Comercio (OMC), mediante la signatura G/TBT/N/ COL/246 del 16 de febrero de 2021.
Que frente al proyecto de resolución se emitió el concepto de abogacía de la competencia de que trata el artículo 7o de la Ley 1340 de 2009, reglamentada por el Decreto número 1074 de 2015 en el que el Superintendente Delegado para la Protección de la Competencia de la Superintendencia de Industria y Comercio mediante radicado de esa Entidad 21- 92948-1-0 del 17 de marzo de 2021, concluyó que: con base en la descripción del Proyecto y el análisis antes referido esta Superintendencia se permite recomendar al Minsalud: Exponer, en la parte considerativa del acto administrativo, las razones técnicas por las que se exceptúan las categorías de alimentos señaladas en los Parágrafos 1o y 2o del artículo 2o del Proyecto. Especificar las razones por las que se justifica excluir a las categorías de alimentos señaladas en los literales a), b), c), f) e i) del Parágrafo 1o del artículo 2o del Proyecto, así como aquellas señaladas en los literales a), b), c), f), i) y m) del parágrafo 2o del artículo 2o del Proyecto. Eliminar del articulado final del Proyecto los literales a), b), c), f) e i) del parágrafo 1o del artículo 2o, así como los literales a), b), c), f), i) y m) del parágrafo 2o del artículo 2o, en el caso en que, de conformidad con la recomendación anterior, no se encuentren las razones técnicas de su inclusión. Definir taxativamente los elementos que se entienden comprendidos dentro de la categoría “jarabes” en el marco de la definición de “azúcares añadidos” contenida en el artículo 3o del Proyecto. Utilizar las expresiones “0”, “cero”, “no contiene”, “libre de”, “sin” y “exento de” que utiliza el Proyecto al referirse al contenido de nutrientes de los alimentos, únicamente para aquellos alimentos que no tienen ningún contenido del nutriente al que se hace referencia. Utilizar el descriptor “bajo en” en aquellos casos en los que se contemplen rangos de tolerancia para determinados nutrientes o componentes presentes en los alimentos, con el fin de evitar posibles asimetrías de información generadas por una declaración errónea del contenido nutricional que confunda al consumidor.
Que en consideración a lo observado por la SIC, es necesario destacar que Colombia hace parte del acuerdo sobre Obstáculos Técnicos al Comercio, en el cual en el artículo 2o, considera el uso de normas internacionales o elementos de esas normas a través de sus reglamentos técnicos, como medio menos restrictivo del comercio para lograr un objetivo legítimo. En este sentido corresponde señalar que el Codex Alimentarius es una referencia normativa internacional en materia de alimentos, y no existe en la actualidad norma Codex de referencia para el tipo de rotulado frontal a la que refiere la medida comunicada. Sin embargo, de acuerdo con la directriz CAC/GL-2-1985, el etiquetado nutricional comprende dos componentes: la declaración de nutrientes y la información nutricional suplementaria.
Que las razones técnicas por las que se exceptúan las anteriores categorías de alimentos se soportan en que la normativa Codex relativa al etiquetado nutricional fue tomada en cuenta para la redacción del presente acto administrativo, resultando por lo tanto las excepciones de constar de etiquetado nutricional y frontal para los productos indicados en el artículo 2o: literales del parágrafo 1o: a), b), c), d), h), i) y j); y para los productos indicados en el artículo 2o: literales del parágrafo 2o: a), b), c), d), g), i), j), k) y m); y las razones que justifican su excepción tienen que ver con que son alimentos que difieren en su composición de una alimentación convencional, por ser alimentos de uso de régimen especial y por otro lado, alimentos en los cuales su contenido nutricional es insignificante y resulta innecesaria su declaración. De otra parte, para los literales del parágrafo 1o: e), f) y k) y del parágrafo 2o: e), f) y l), es importante, mencionar que la OPS afirma que: la decisión de no incluir los alimentos sin procesar o mínimamente procesados, y sin adición de sodio, grasas o azúcares y los platos recién preparados con estos alimentos e ingredientes se fundamenta en estudios poblacionales realizados en varios países de las Américas que muestran que los regímenes alimentarios basados en esos alimentos, ingredientes y platos en general se ciñen a las metas de ingesta de nutrientes de la población de la OMS, así las cosas, Colombia, adoptó tales directrices. Finalmente, para la excepción: g) del parágrafo 1o y h) del parágrafo 2o, se realiza con base en la imposibilidad de incluir la información nutricional en un envase de origen natural, tal como sucede en una hoja de plátano. Ahora bien, los descriptores “0”, “cero”, “no contiene”, “libre de”, “sin”, “exento de”, “bajo en”, fueron tomados de la normativa Codex CAC/GL-2-1985, y resultan de la imposibilidad de un alimento de llegar a un cero absoluto en tales nutrientes, sin embargo, los límites utilizados en estas expresiones son los más bajos a los que se pueda llegar. De otra parte, para finalizar con la totalidad de las recomendaciones, se acoge la observación de la SIC de incluir la definición de jarabes en este reglamento.
Que de acuerdo al numeral 2 del artículo 1o de la Ley 962 de 2005, modificado por el artículo 39 del Decreto-ley 019 de 2012 y el artículo 3o del Decreto número 2106 de 2019, este Ministerio solicitó concepto al Departamento Administrativo de Función Pública, el cual surtió concepto bajo el radicado número 20215010144911 y afirma lo siguiente: “sobre este reglamento técnico se encuentra que no corresponde con un trámite, sino con las condiciones y especificaciones que deben ser observadas en el etiquetado nutricional y frontal que aplica a todos los alimentos para consumo humano envasados o empacados, nacionales e importados que se comercialicen en el territorio nacional, con las excepciones previstas en el citado reglamento; y el Ministerio puede continuar con las gestiones relacionadas con su expedición”.
Que de conformidad con lo anterior, se hace necesario establecer un reglamento técnico que garantice los requisitos sanitarios que deben cumplir los alimentos envasados o empacados para consumo humano, como una medida necesaria para proporcionar al consumidor información nutricional clara y comprensible, con el fin de promocionar la alimentación balanceada y saludable y proteger la salud humana y prevenir posibles daños a la misma.
En mérito de lo expuesto,
RESUELVE:
OBJETO, CAMPO DE APLICACIÓN Y DEFINICIONES.
ARTÍCULO 1o. OBJETO. La presente resolución tiene por objeto establecer el reglamento técnico a través del cual se disponen las condiciones y requisitos que debe cumplir el etiquetado o rotulado nutricional y frontal de advertencia de los alimentos y bebidas envasadas o empacadas para consumo humano, con el propósito de proporcionar al consumidor final una información nutricional lo suficientemente clara y comprensible sobre el producto, y prevenir prácticas que induzcan a engaño o error y permitir al consumidor efectuar una elección informada.
ARTÍCULO 2o. CAMPO DE APLICACIÓN. <Artículo modificado por el artículo 1 de la Resolución 2492 de 2022. El nuevo texto es el siguiente:> Las disposiciones establecidas en la presente resolución aplican a todos los alimentos para consumo humano envasados y productos alimenticios procesados y ultraprocesados envasados o empacados, nacionales e importados que se comercialicen en el territorio nacional.
2.1. Se exceptúan de la aplicación del etiquetado nutricional, los siguientes alimentos:
a) Fórmula infantil para niños o niñas entre 0 y 6 meses.
b) Fórmula infantil para niños o niñas entre 6 y 12 meses.
c) Fórmula infantil especial.
d) Alimentos para Propósitos Médicos Especiales (Apmes).
e) Productos de un solo ingrediente y que no contengan aditivos adicionales.
f) Alimentos con envase de materiales de origen natural.
g) Infusiones de hierbas y frutas; té, té descafeinado, té instantáneo o soluble, o extracto de té, extracto de té descafeinado; café descafeinado, café molido, café instantáneo o soluble, o extracto de café, o extracto de café descafeinados, que no contengan ingredientes añadidos.
h) Alimentos a granel.
i) Alimentos utilizados como materia prima para la industria y los ingredientes secundarios que no se venden directamente al consumidor.
j) Especias o condimentos vegetales, a los que no se les haya adicionado sal o aditivos con sodio, grasas o azúcares.
k) Alimentos sin procesar.
l) Alimentos mínimamente procesados.
m) Alimentos y bebidas típicos o artesanales.
2.2. Se exceptúan de la aplicación del etiquetado frontal de advertencia, los siguientes alimentos:
a) Fórmula infantil para niños o niñas entre 0 y 6 meses.
b) Fórmula infantil para niños o niñas entre 6 y 12 meses.
c) Fórmula infantil especial.
d) Alimentos para Propósitos Médicos Especiales (Apmes).
e) Productos de un solo ingrediente y que no contengan aditivos adicionales.
f) Sal yodada y fluorizada, y sucedáneos de la sal.
g) Alimentos con envase de materiales de origen natural.
h) Infusiones de hierbas y frutas, té, té descafeinado, té instantáneo o soluble, o extracto de té; o extracto de té descafeinados, y café descafeinado., café instantáneo o soluble, o extracto de café; o extracto de café descafeinados que no contengan ingredientes añadidos.
i) Alimentos a granel.
j) Alimentos utilizados como materia prima para la industria y los ingredientes secundarios que no se venden directamente al consumidor.
k) Alimentos envasados a los que no se les haya adicionado sal/sodio y/o grasas o azúcares.
l) Bebidas hidratantes – energéticas para deportistas.
m) Alimentos sin procesar
n) Alimentos mínimamente procesados
o) Alimentos y bebibles típicos o artesanales
El fabricante que desee realizar declaraciones de nutrientes, de propiedades nutricionales o de salud, respecto de los alimentos anteriormente excluidos deberá dar cumplimiento a lo establecido en el presente reglamento técnico.
PARÁGRAFO 1o. La carne cruda envasada a la que se le han agregado productos alimenticios, condimentos o aditivos que contengan sal o sodio, únicamente deben declarar el contenido de sodio y, si este supera el límite establecido en el artículo 32 del presente acto administrativo, deberá etiquetar el sello frontal de advertencia de sodio. La tabla nutricional debe ser de al menos el 15% del área donde se ubique.
PARÁGRAFO 2o. Para los productos de peso variable, no les aplica la inclusión de porciones por envase en la tabla nutricional, ni en la cara principal de exhibición del envase.
ARTÍCULO 3o. DEFINICIONES. <Artículo modificado por el artículo 2 de la Resolución 2492 de 2022. El nuevo texto es el siguiente:> Para la aplicación de la presente resolución, se adoptan las siguientes definiciones:
3.1. Ácidos grasos esenciales: Nutrientes que requiere y no puede sintetizar el organismo del ser humano, por lo que deben ser suministrados en la dieta. Los ácidos grasos esenciales son linoleico y alfa-linolénico, así como EPA (ácido eicosapentaenoico) y DHA (ácido docosahexanoico), que debido a que su tasa de conversión es muy baja, deben suministrarse en la alimentación.
3.2. Alimentos mínimamente procesados: Alimentos sin procesar que han sido sometidos a limpieza, remoción de partes no comestibles o no deseadas, secado, molienda, fraccionamiento, tostado, escaldado, pasteurización, enfriamiento, congelación, envasado al vacío o fermentación no alcohólica. Los alimentos mínimamente procesados también incluyen combinaciones de dos o más alimentos, sin procesar o mínimamente procesados, y que pueden ser adicionados con vitaminas y minerales para restablecer el contenido original de micronutrientes o para fines de salud pública. Estos alimentos no pueden ser adicionados con sal/sodio, grasas o azúcares o aditivos que los contengan, incluyen, pero no se limitan a: frutas frescas partidas, secas, refrigeradas o congeladas; verduras, granos y leguminosas, secas, refrigeradas o congeladas; nueces; productos cárnicos comestibles, refrigerados o congelados, productos de la pesca, refrigerados o congelados; huevos y leche.
3.3. Alimentos y bebidas típicos o artesanales: Alimentos envasados que cumplan con los siguientes requisitos: (i) Elaborado a partir de prácticas tradicionales no industrializadas, (ii) que correspondan a la tradición cultural de las regiones del país y (iii) dando cumplimiento gradual a las condiciones de inocuidad de acuerdo con las disposiciones de los artículos 3o y 7o de la Ley 2254 de 2022, o la que modifique o sustituya.
3.4. Alimentos sin procesar: Alimentos obtenidos directamente de plantas o animales que no son sometidos a ninguna modificación física o química desde el momento en que son extraídos de fa naturaleza hasta su preparación culinaria o consumo. También pueden nombrarse como alimentos frescos o naturales
3.5. Área total disponible de impresión: Área total de la etiqueta menos los selles posteriores.
3.6. Azúcares totales: Carbohidratos tipo monosacáridos y disacáridos presentes de forma natural en los alimentos o añadidos a los mismos.
3.7. Azúcares añadidos: Son los azúcares adicionados o agregados, incluyendo a los azúcares que se adicionan durante el procesamiento de alimentos o se empaquetan como tales, e incluyen azúcares como monosacáridos y disacáridos, aquellos contenidos en los jarabes y los naturalmente presentes en la miel y en los concentrados de jugos de frutas o vegetales. Estos no incluyen los azúcares intrínsecos que se encuentran en la leche, frutas y los vegetales y los azúcares que son carbohidratos no glucémicos.
3.8. Carbohidratos totales: Todos los monos, di, aligo y polisacáridos, incluidos los polialcoholes y la fibra presentes en el alimento.
3.9. Carbohidratos disponibles o glucémicos: Total de carbohidratos del alimento menos el contenido de fibra dietaria, polialcoholes y carbohidratos no glucémicos.
3.10. Carbohidratos no disponibles o no glucémicos: Carbohidratos que presentan diversas formas químicas, y aunque se digieren, no proporcionan glucosa para el metabolismo celular. Deben demostrar un índice glucémico inferior a 15, correspondiente al menor valor presentado por un carbohidrato glucémico (fructosa).
3.11. Colesterol: Sustancia tipo esterol presente en las grasas de origen animal.
3.12. Declaración de función de los nutrientes: Son declaraciones de propiedades que describen la función fisiológica del nutriente en el crecimiento, el desarrollo y las funciones normales del organismo.
3.13. Declaración de nutrientes: Relación o enumeración normalizada del contenido de nutrientes de un alimento.
3.14. Declaraciones de propiedades de otras funciones: Conciernen a efectos benéficos específicos del consumo de alimentos y sus constituyentes (nutritivos y no nutritivos) sobre las funciones fisiológicas o las actividades biológicas, pero no incluyen declaraciones de propiedades de función de nutrientes. Tales declaraciones de propiedades se relacionan a una contribución positiva a la salud o a una condición relacionada con la salud, o al mejoramiento de una función, o a la modificación o preservación de la salud.
3.15. Declaración de propiedades de salud: Cualquier representación que declare, sugiera o implique que existe una relación entre un alimento o un constituyente/ componente de dicho alimento, y la salud.
3.16. Declaración de propiedades nutricionales: Cualquier representación que afirme, sugiera o implique que un producto posee propiedades nutricionales particulares, incluyendo, pero no limitándose a su valor energético y contenido de proteínas, grasas, carbohidratos y fibra dietaria, así como, su contenido de vitaminas y minerales. No constituirán declaración de propiedades nutricionales: la mención de sustancias en la lista de ingredientes, ni el nombre o marca del alimento envasado o la mención de nutrientes como parte obligatoria del etiquetado nutricional o la declaración cuantitativa o cualitativa de algunos nutrientes o ingredientes en el rótulo o etiqueta.
3.17. Declaraciones de propiedades de reducción de riesgos de enfermedad: Son declaraciones de propiedades relacionadas con el consumo de un alimento o de un componente de dicho alimento en el contexto de una dieta total, que puede ayudar a la reducción del riesgo de una enfermedad o condición relacionada con la salud. La reducción de riesgos significa el alterar de manera significativa un factor o factores mayores de riesgo reconocidos como involucrados en el desarrollo de una enfermedad crónica o condición adversa relacionada a la salud.
3.18. Dieta total: Alimentación habitual de una persona o población.
3.19. Edulcorantes: Cualquier sustancia diferente a los azúcares añadidos y/o libres que confiera un sabor dulce.
3.20. Envasados con peso variable: Envasados en los cuales el contenido es medido, empacado, rotulado individualmente y cada empaque tiene un peso y/o volumen diferente.
3.21. Envase de materiales de origen natural: Elemento diseñado para contener un alimento que incluye, pero no se limita a hojas de plátano, hojas de bijao, hojas de maíz, totumos.
3.22. Fibra dietaria o dietética: carbohidratos comestibles que no se digieren ni se absorben en el intestino delgado del ser humano. La fibra dietética consta de uno o varios de los siguientes carbohidratos: carbohidratos comestibles que se encuentran naturalmente en los alimentos en la forma en que se consumen, carbohidratos obtenidos de materia prima alimentaria por medios físicos, enzimáticos o químicos y carbohidratos sintéticos.
3.23. Fibra insoluble: Es la fracción de la fibra dietaria que no se disuelve en agua.
3.24. Fibra soluble: La fracción de la fibra dietaria que se disuelve en agua.
3.25. Fórmula infantil para niños entre 0 y 6 meses: Producto en forma líquida o en polvo destinado a la alimentación de los niños o niñas de 0 a 6 meses de edad, utilizado cuando sea indicado por un profesional de la salud, que por sí solo, cubre las necesidades nutricionales del niño o la niña, como principal fuente líquida de alimentación hasta la introducción de la alimentación complementaria, para casos en que no sea posible la lactancia materna.
3.26. Fórmula infantil para niños entre 6 y 12 meses: Producto en forma líquida o en polvo, especialmente fabricado según las necesidades nutricionales de los niños o niñas entre los 6 y 12 meses de edad, utilizado cuando sea indicado por un profesional de la salud, en conjunto con la alimentación complementaria.
3.27. Fórmula infantil especial: Producto en forma líquida o en polvo cuya composición ha sido modificada para abordar determinados trastornos o afecciones fisiológicas durante los primeros meses de vida e incluso después de la introducción de una alimentación complementaria.
3.28. Fortificación voluntaria de nutrientes: Proceso por el cual los fabricantes de alimentos deciden añadir unos nutrientes esenciales específicos a determinados alimentos o determinadas categorías de alimentos.
3.29. Grasa total: Sumatoria de grasa saturada, grasa monoinsaturada, grasa poliinsaturada e incluye las grasas trans.
3.30. Grasas o lípidos: Sustancias insolubles en agua y solubles en solventes orgánicos, constituidas especialmente por esteres de los ácidos grasos. Este término incluye triglicéridos, fosfolípidos, glicolípidos, ceras y esteroles.
3.31. Grasa saturada o ácidos grasos saturados: Aquellos que no presentan dobles enlaces en su cadena hidrocarbonada.
3.32. Grasa monoinsaturada o ácidos grasos monoinsaturados: Aquellos que presentan un doble enlace, en su cadena hidrocarbonada. Para efectos de rotulado o etiquetado se entenderá como grasa monoinsaturada aquella que presenta doble enlace en su configuración Cis.
3.33. Grasa poliinsaturada o ácidos grasos poliinsaturados: Aquellos que presentan dos o más dobles enlaces en su cadena hidrocarbonada. Para efectos de rotulado o etiquetado se entenderá como grasa poliinsaturada aquella que presenta los dobles enlace en su configuración Cis.
3.34. Grasa transisómera o trans o ácidos grasos trans: Todos los isómeros geométricos de ácidos grasos monoinsaturados y poliinsaturados que poseen, en la configuración trans, uno o más dobles enlaces carbonocarbono no conjugados. Para efectos de etiquetado o rotulado se entenderá como grasa trans la sumatoria de todos los isómeros mono y poliinsaturados en configuración trans que atienden a lo descrito anteriormente.
3.35. Índice glucémico: Se define como el área incremental bajo la curva de respuesta de glucosa en sangre a partir de una porción de 50 g de carbohidratos de un alimento de prueba, expresada como un porcentaje de la respuesta a la misma cantidad de carbohidratos de un alimento estándar (pan blanco o glucosa) consumido por el mismo sujeto. Este valor sólo se considera válido cuando se determina de forma directa siguiendo el protocolo oficial establecido por el Panel de Expertos FAO/OMS, por tratarse de una prueba biológica susceptible a diferentes factores.
3.36. Jarabes: Líquidos viscosos constituidos por solución de azúcares en agua o en zumos de frutas o bien por mezcla de estos, con o sin agentes aromáticos y aditivos autorizados.
3.37. Medida casera: Son utensilios o formas comúnmente utilizados por el consumidor para medir alimentos, incluyendo, pero no limitándose a: taza, vaso, rebanada, unidad, cucharada, cucharadita.
3.38. Minerales: Sustancias inorgánicas necesarias para los procesos fisiológicos y que no son fuente de energía.
3.39. Nutriente: Cualquier sustancia química consumida normalmente como componente de un alimento que es necesaria para el crecimiento, el desarrollo y/o el mantenimiento de la salud, o cuya carencia hará que se produzcan cambios químicos o fisiológicos característicos.
3.40. Nutriente esencial: Nutriente que no es sintetizado por el organismo o es sintetizado en cantidades insuficientes y que debe ser consumido para garantizar el crecimiento, desarrollo y/o mantenimiento de la salud.
3.41. Porción: Es la cantidad de un alimento normalmente consumida en una ocasión por personas mayores de 4 años y adultos o por niños mayores de 6 meses y menores de 4 años, que debe declararse en la etiqueta y se expresa usando medidas caseras comunes apropiadas para ese alimento.
3.42. Prebióticos: Sustratos que son utilizados selectivamente por microorganismos huéspedes que confieren un beneficio para la salud.
3.43. Probióticos: Microorganismos vivos que, cuando se administran en cantidades apropiadas, confieren al huésped un beneficio para la salud.
3.44. Productos alimenticios procesados: Productos alimenticios elaborados con procesos tecnológicos, sometidos a procesos de transformación se les puede añadir dos o más ingredientes como sal, azúcar, grasas u otros. Tienen de dos o más ingredientes o aditivos y más del 50% de los ingredientes son alimentos sin procesar o mínimamente procesados.
3.45. Productos alimenticios ultraprocesados: Productos alimenticios elaborados con procesos tecnológicos, sometidos a procesos de transformación a los cuales se les añade sal, azúcar, grasas u otros ingredientes. Tienen más de 5 ingredientes y/o aditivos y menos del 50% de los ingredientes son alimentos sin procesar o mínimamente procesados. Dentro de sus ingredientes se incluyen, pero no se limitan a: caseína, suero de leche, hidrolizado de proteína, proteínas aisladas de soja, aceites hidrogenados, parcialmente hidrogenados o interesterificados, almidones modificados.
3.46. Producto de un solo ingrediente: Alimento envasado en el que en su lista de ingredientes sólo contenga un ingrediente, incluyendo, pero no limitándose a agua envasada, café, granos de café molido, azúcar, aceite de oliva.
3.47. Producto reconstituido: Aquel que por su naturaleza de consumo debe ser reconstituido en algún solvente comestible ya sea para obtener un producto sólido, semisólido o un líquido, listo para consumir.
3.48. Proteína: son polímeros de L-alfa aminoácidos unidos por enlaces peptidicos. Las proteínas se denominan simples cuando están constituidas únicamente por aminoácidos, y compuestas cuando incluyen otras sustancias como lípidos, carbohidratos, minerales, entre otros.
3.49. Respuesta glucémica: El grado del cambio o gradiente en el contenido de glucosa en sangre, después del consumo de un carbohidrato de prueba en una bebida o un alimento, en relación con un estándar como la glucosa.
3.50. Rotulado o etiquetado nutricional: Toda descripción contenida en el rótulo o etiqueta de un alimento destinada a informar al consumidor sobre el contenido de nutrientes, propiedades nutricionales y propiedades de salud de un alimento.
3.51. Rotulado o etiquetado frontal de advertencia: Sistema de información situado en la cara principal de exhibición, el cual muestra de manera veraz, clara, rápida y sencilla, cuando un producto envasado presenta contenidos excesivos de nutrientes de interés en salud pública (azúcares, grasa saturada, grasa trans, sodio) y la presencia de edulcorantes.
3.52. Sello positivo: Logo de visto bueno que indica que el alimento contiene contenidos bajos de los nutrientes de interés en salud pública (azúcares añadidos, grasa saturada y sodio) y que no usan edulcorantes en su formulación.
3.53. Simbióticos: Se entiende como la combinación de sustancias prebióticas con cultivos probióticos que se encuentran presentes en un mismo alimento.
3.54. Tiempo de comida principal: En el marco de la planificación diaria de la alimentación, hace referencia a los momentos en los que se distribuyen los alimentos en mayor proporción, a saber, desayuno, almuerzo y cena.
3.55. Valores de Referencia de Nutrientes (VRN) o Valor de Referencia: Son un conjunto de valores numéricos que están basados en datos científicos para efectos de etiquetado o rotulado nutricional y declaraciones de propiedades pertinentes. Comprenden estos dos tipos de VRN:
a) Valores de referencia de nutrientes - necesidades (VRN-N): Son aquellos que hacen alusión a los VRN basados en niveles de nutrientes asociados a necesidades de nutrientes.
b) Valores de referencia de nutrientes - enfermedades no transmisibles (VRN-ENT): Son aquellos que hacen alusión a los VRN basados en niveles de nutrientes asociados a la reducción del riesgo de enfermedades no transmisibles relativas al régimen alimentario, excluyendo las enfermedades o trastornos provocados por carencias de nutrientes.
3.56. Vitaminas: Sustancias orgánicas esenciales para el mantenimiento de la salud, crecimiento y funcionamiento corporal normal. Se requieren en pequeñas cantidades y no son fuente de energía.
ARTÍCULO 4o. ALCANCE. El etiquetado nutricional comprende la declaración de nutrientes y la información nutricional complementaria, la cual incluye, las declaraciones de propiedades nutricionales, las declaraciones de propiedades de salud y el etiquetado frontal.
ARTÍCULO 5o. PROPÓSITOS Y CARACTERÍSTICAS DEL ETIQUETADO O ROTULADO NUTRICIONAL. El etiquetado nutricional deberá realizarse con el cumplimiento de las siguientes características:
5.1 Proporcionar un medio eficaz para indicar el contenido de nutrientes del alimento en la etiqueta, facilitando al consumidor la toma de una decisión informada
5.2 La información no deberá describir o presentar el alimento de forma falsa, equívoca o engañosa o susceptible de crear en modo alguno una impresión errónea respecto de su contenido nutricional, propiedades nutricionales y de salud, en ningún aspecto.
5.3 La información no debe llevar a los consumidores a creer que existe un conocimiento cuantitativo exacto de lo que las personas deben comer con el fin de mantener la salud, sino que debe dar a conocer la cantidad de nutrientes que contiene el producto. Una delimitación cuantitativa más exacta para los individuos no es válida, porque no hay manera significativa de que el conocimiento acerca de los requerimientos individuales se pueda utilizar en el etiquetado.
5.4 Aplicar los principios nutricionales basados en la evidencia científica fuerte y bajo la ética y responsabilidad social, sin conflictos de interés en el diseño, producción y elaboración de productos alimentarios, en beneficio de la salud pública.
5.5 Toda la información presentada en la etiqueta debe ser completa, veraz, verificable, que no induzca a confusión o engaño.
5.6 Garantizar que la información presentada en la etiqueta no se contraponga a la promoción de hábitos alimentarios saludables en concordancia con las políticas de salud pública existentes para tal fin.
ARTÍCULO 6o. PROHIBICIONES EN EL ROTULADO O ETIQUETADO NUTRICIONAL. En el etiquetado nutricional está prohibido el uso de las siguientes declaraciones:
6.1 De propiedades nutricionales o de salud, que no estén basadas en evidencia científica.
6.2 Que indiquen, representen, sugieran o impliquen que el alimento es útil, adecuado o efectivo para aliviar, tratar o curar cualquier enfermedad o trastorno fisiológico.
6.3 Que las Asociaciones (Médicas o de Salud) avalen productos alimentarios con fines de publicidad y mercadeo.
6.4 Que promuevan el consumo excesivo de cualquier alimento.
6.5 Que sea contrario a los hábitos alimentarios saludables establecidos en las políticas de salud pública existentes para tal fin.
6.6 Afirmar que el alimento por sí solo adecua totalmente las recomendaciones de ingesta de energía y nutrientes, o que por sí solo puede sustituir algún tiempo de comida principal.
6.7 Que expresen o sugerirá que la ingesta de los alimentos, cualquiera de sus ingredientes o nutrientes proporciona a las personas características o habilidades extraordinarias.
DECLARACIÓN DE NUTRIENTES.
ARTÍCULO 7o. APLICACIÓN DE LA DECLARACIÓN DE NUTRIENTES. La declaración de nutrientes será obligatoria para todo alimento envasado o empacado objeto de esta resolución y deberá cumplir las disposiciones del presente capítulo incluyendo la tabla de información nutricional contemplada en el Capítulo VI del presente reglamento, salvo para los alimentos exceptuados en el artículo 2o.
ARTÍCULO 8o. DECLARACIÓN Y FORMA DE PRESENTACIÓN DE LOS NUTRIENTES. En la tabla de información nutricional únicamente se permite: la declaración de los nutrientes obligatorios, de los opcionales, acorde a lo establecido en el presente capítulo. La declaración del contenido de nutrientes debe hacerse en forma numérica.
ARTÍCULO 9o. EXPRESIÓN DE LOS VALORES. Los nutrientes serán declarados de acuerdo con lo establecido en la siguiente tabla. Se utilizará la aproximación matemática al número entero o decimal más cercano, como se observa en la siguiente tabla 1:
Tabla 1. Expresión de valores
| Rangos de valores | Forma de expresión | Aproximación matemática (ejemplo) |
| Valores mayores o iguales a 1000 | se declararán en números enteros con cuatro cifras | 1136.4 se aproxima a 1136 1136.8 se aproxima a 1137 |
| Valores mayores o iguales a 100 | se declararán en números enteros con tres cifras | 237.8 se aproxima a 238 237.3 se aproxima a 237 |
| Valores menores a 100 y mayores o iguales a 10 | se declararán en números enteros con dos cifras | 54.6 se aproxima a 55 54.2 se aproxima a 54 |
| Valores menores a 10 y mayores o iguales a 1 | se declarará con una cifra decimal | 9.82 se aproxima a 9.8 9.87 se aproxima a 9.9 |
| Valores menores a 1 | Se declarará para las vitaminas y minerales con dos cifras decimales y con una cifra decimal para el resto de los nutrientes. | 0.843 se aproxima a 0.84 0.848 se aproxima a 0.85 |
PARÁGRAFO 1o. Si el valor es exactamente la mitad del intervalo establecido se aproxima al número superior más cercano.
PARÁGRAFO 2o. En la información nutricional, se expresará “cero” o “0” o “no contiene” para el valor energético y/o nutrientes, cuando el alimento contenga cantidades menores o iguales a las establecidas como “no significativas” de acuerdo con la tabla siguiente
Tabla 2. Cantidades no significativas
| Valor energético o nutriente | Cantidades no significativas por 100 g o 100 mL (expresada en kcal, g o mg) |
| Calorías | Menor o igual que 4 kcal o menor que 17 kJ |
| Carbohidratos totales | Menor o igual que 0.5 g |
| Azúcares totales | Menor o igual que 0.5 g |
| Proteínas | Menor o igual que 0.5 g |
| Grasa total | Menor o igual que 0.5 g |
| Grasa saturada | Menor o igual que 0.1 g |
| Grasa trans | Menor o igual que 100 mg |
| Colesterol | Menor o igual que 5 mg |
| Fibra dietaria | Menor o igual que 0.5 g |
| Sodio | Menor o igual que 5 mg |
ARTÍCULO 10. CONDICIONES GENERALES PARA LA DECLARACIÓN DE NUTRIENTES. La declaración de nutrientes cumplirá las siguientes condiciones generales:
10.1 La declaración de los nutrientes debe hacerse por 100 g del alimento y por porción, para alimentos sólidos y semisólidos, y por 100 mL de producto y por porción para alimentos líquidos.
10.2 En el caso de productos reconstituidos se entenderá como sólido, semisólido o liquido acorde a las condiciones de uso definidas y recomendadas por el fabricante. Podrán incluirse dos declaraciones en caso que se sugieran varios líquidos para reconstituir (ejemplo agua y leche).
10.3 La declaración del contenido de nutrientes debe hacerse con base en las expresiones establecidas en el artículo 9o.
10.4 El número de porciones por empaque debe estar declarado en la cara principal de exhibición de la etiqueta, junto al contenido neto del alimento o bebida. El tamaño de esta leyenda debe estar acorde al tamaño del contenido neto, establecido en el anexo técnico de la Resolución 5109 de 2005 o aquella que la modifique o sustituya.
10.5 Los valores de los nutrientes que figuren en la tabla de información nutricional deben ser valores promedios obtenidos de análisis de muestras o valores de una muestra que sean representativas del producto que ha de ser rotulado o etiquetado o tomados de la Tabla de Composición de Alimentos Colombianos del ICBF, o de publicaciones internacionales, o de otras fuentes de información tales como, especificaciones del contenido nutricional de ingredientes utilizados en la formulación del producto. Sin embargo, los valores de nutrientes que fundamenten las declaraciones de propiedades nutricionales o de salud deben ser obtenidos mediante pruebas analíticas. Este proceso se debe repetir cuando haya alguna modificación en el aporte nutricional y ficha técnica, previamente autorizada por el Invima. El fabricante es responsable de la veracidad de los valores declarados.
10.6 Se deben cumplir los siguientes criterios:
a) Nutrientes adicionados al alimento: El contenido de vitaminas, minerales, proteína, fibra dietaria, grasa monoinsaturada o poliinsaturada, debe ser mínimo el 80% del valor declarado en la etiqueta.
b) Nutrientes presentes naturalmente en el alimento: El contenido de vitaminas, minerales, proteína, carbohidrato total, fibra dietaria, otro carbohidrato, grasa monoinsaturada o poliinsaturada, debe ser mínimo el 80% del valor declarado en la etiqueta. En el caso de calorías, azúcares, grasa total, grasa saturada, grasa trans, colesterol o sodio se acepta un exceso no mayor del 20% sobre el valor declarado en la etiqueta.
c) Para determinar el contenido de nutrientes, se debe garantizar que los métodos analíticos utilizados cumplan con los requisitos particulares para su uso específico, utilicen metodologías avaladas por organismos internacionales, regionales o nacionales competentes en este campo, lo cual será verificado por la autoridad sanitaria.
d) En alimentos envasados o empacados en agua, salmuera o aceite, cuyo líquido normalmente no es consumido, la declaración de nutrientes debe hacerse con base en la masa escurrida o sólido drenado.
10.7 Nutrientes de declaración obligatoria:
Deberán declararse obligatoriamente en la tabla nutricional, el valor energético y las cantidades de los nutrientes que se indican a continuación, por 100 g del alimento y por porción para alimentos sólidos, y por 100 mL de producto y por porción para alimentos líquidos y con lo establecido en el artículo 9o, del presente reglamento técnico. En el caso de productos reconstituidos se declarará considerando el producto preparado en condiciones de consumo recomendadas por el fabricante:
Tabla 3. Formas de expresión de los nutrientes de declaración obligatoria
| Nutriente | Forma de expresión | Requisitos adicionales |
| Energía | El valor energético debe expresarse en kilocalorías (kcal) y opcionalmente en kilojulios (kJ). Para su declaración podrán utilizarse los términos o expresiones energía, valor energético, contenido energético, kilocalorías, calorías, Calorías, calorías totales. | La cantidad de calorías totales será la sumatoria de las calorías aportadas por la grasa, carbohidratos totales, proteínas y fibra dietaria, más otras fuentes de energía consideradas en el artículo 11 el presente reglamento, obtenidas a partir de las cantidades de estos nutrientes, declaradas en la tabla nutricional según los criterios del numeral 10.4. |
| Proteína | Debe expresarse en gramos | |
| Nutriente | Forma de expresión | Requisitos adicionales |
| Grasa total | Debe expresarse en gramos | Cuando se haga una declaración de propiedades nutricionales respecto a la cantidad o el tipo de ácidos grasos, debe indicarse inmediatamente a continuación de la declaración del contenido de grasa total, las cantidades de ácidos grasos saturados, monoinsaturados, poliinsaturados, trans y colesterol. |
| Grasa saturada | Debe expresarse en gramos | La declaración de grasa saturada no es obligatoria para alimentos que contienen menos de 0.1 g de grasa saturada por 100 g o 100 mL a menos que se hagan declaraciones de propiedades nutricionales sobre el contenido de grasa total, ácidos grasos o colesterol. Si la grasa saturada no se declara deberá figurar al final de la tabla de Información Nutricional la expresión “No es una fuente significativa de grasa saturada” |
| Grasa trans | Debe expresarse en miligramos | - |
| Carbohidratos totales | Debe expresarse en gramos | - |
| Azúcares totales | Debe expresarse en gramos | La declaración de azúcares totales no es obligatoria para alimentos que contienen menos de 0.5 g de azúcares por 100 g de alimentos, a excepción del caso en que se haga alguna declaración o referencia sobre edulcorantes artificiales, azúcares o polialcoholes en la etiqueta; en este caso el azúcar se declarará como cero (0). Si los azúcares no se declaran deberá figurar al final de la tabla de Información Nutricional la expresión “No es una fuente significativa de azúcares” |
| Azúcares añadidos | Debe expresarse en gramos | - |
| Fibra dietaria | Debe expresarse en gramos | La declaración de fibra dietaria no es obligatoria para alimentos que contienen menos de 0.5 g de fibra dietaria por 100 g de alimentos. Cuando se haga una declaración de propiedades nutricionales respecto de la fibra dietaria debe indicarse la cantidad de sus fracciones soluble e insoluble. |
| Sodio | Debe expresarse en miligramos | - |
| Vitamina A | Debe expresarse en microgramos de ER | La declaración de vitamina A, vitamina D, hierro y zinc no es obligatoria para alimentos que contienen cantidades inferiores al 2% del valor de referencia por 100 g del alimento. Si estas vitaminas y minerales no se declaran, deberá figurar al final de la Tabla de Información Nutricional cualquiera de las siguientes expresiones: “contiene menos del 2% de…” o “No es una fuente significativa de…” seguido de las vitaminas y minerales que no se declaran. |
| Vitamina D | Debe expresarse en microgramos o Unidades Internacionales | |
| Hierro | Debe expresarse en miligramos | |
| Zinc | Debe expresarse en miligramos | |
| Calcio | Debe expresarse en miligramos | |
PARÁGRAFO. Si el alimento tiene una cantidad menor a la cantidad significativa de los anteriores nutrientes, de acuerdo con la tabla 2, del presente reglamento, no es necesario su declaración.
10.7.1. Vitaminas y minerales diferentes de la vitamina A, vitamina D, hierro, calcio y zinc. Vitaminas y minerales diferentes de la vitamina A, vitamina D, hierro, calcio y zinc se pueden declarar cuando se han establecido valores de referencia en el Capítulo III de este reglamento y hayan sido adicionados o estén presentes naturalmente en el alimento en cantidades iguales o superiores al 2% del valor de referencia por 100 g o 100 mL del alimento.
10.8 Nutrientes de declaración opcional. Se podrán declarar opcionalmente los nutrientes indicados a continuación. No obstante, cualquier declaración de propiedad nutricional sobre los mismos implica que la declaración del nutriente deja de ser opcional y se convierte en obligatoria, lo cual implica el cumplimiento de lo establecido en el presente acto administrativo.
PARÁGRAFO. Para el caso de los nutrientes que no tengan valor de referencia y el fabricante desee declararlos, debe realizar una solicitud a la Sala Especializada de Alimentos y Bebidas del Invima, con el objetivo de obtener su aprobación para incluir la declaración.
10.8.1 Grasa monoinsaturada, poliinsaturada, fibra soluble e insoluble y polialcoholes, colesterol y potasio. Las cantidades de grasa monoinsaturada, poliinsaturada, fibra soluble e insoluble y polialcoholes, debe expresarse en gramos y el colesterol y potasio en miligramos. Por porción y por 100 g de alimento sólido y en gramos por porción y por 100 mL de alimento líquido, según lo establecido en el artículo 9o del presente reglamento técnico. En el caso de productos reconstituidos se declarará considerando el producto preparado en condiciones de consumo recomendadas por el fabricante.
ARTÍCULO 11. CÁLCULO DE ENERGÍA Y NUTRIENTES. La cantidad de calorías totales será la sumatoria de las calorías aportadas por la grasa, carbohidratos, proteínas y fibra dietaria, obtenidas a partir de las cantidades de estos nutrientes declarados en la tabla nutricional. Para el cálculo de energía y nutrientes se tendrán en cuenta los siguientes criterios:
11.1 Energía. La cantidad de energía que ha de declararse debe calcularse utilizando los siguientes factores de conversión:
Tabla 4. Factores de conversión
| Carbohidratos disponibles | 4 kcal/g (17 kJ/g) |
| Proteínas | 4 kcal/g (17 kJ/g) |
| Grasas | 9 kcal/g (37 kJ/g) |
| Alcohol (Etanol) | 7 kcal/g (29 kJ/g) |
| Ácidos orgánicos | 3 kcal/g (13 kJ/g) |
| Carbohidratos no glucémicos | Ver literal c) del presente artículo |
a) Para fibra dietaria, el fabricante utilizará los factores de conversión calórica contemplados en documentos de referencia científica nacional o internacional;
b) Para polialcoholes como sorbitol, manitol, xilitol y otros, el fabricante utilizará los factores de conversión calórica contemplados en documentos de referencia científica nacional o internacional.
c) Para el caso de los carbohidratos no glucémicos, el fabricante utilizará los factores de conversión calórica contemplados en documentos avalados por organismos científicos del orden nacional o internacional competentes en este campo. En caso de no existir estas referencias, el fabricante deberá realizar la solicitud a la Sala Especializada de Alimentos y Bebidas del Invima, con la respectiva evidencia científica frente al factor de conversión.
11.2 Proteínas. La cantidad de proteínas que ha de declararse debe calcularse utilizando la fórmula siguiente: Proteína = contenido total de nitrógeno Kjeldahl x 6,25, a no ser que se dé un factor diferente en normas internacionales o en el método de análisis para un alimento.
11.3 Carbohidratos Totales. Los carbohidratos totales se calculan por sustracción de la proteína, la grasa total, la humedad y la ceniza, de la masa total del alimento.
ARTÍCULO 12. TAMAÑOS Y CARACTERÍSTICAS DE LAS PORCIONES. A efectos de lograr una estandarización del tamaño de la porción para ser usada en el rotulado o etiquetado nutricional por porción, debe efectuarse de acuerdo con los siguientes requisitos:
12.1 El tamaño de la porción declarada en la etiqueta de un alimento debe ser determinado a partir de las cantidades de referencia normalmente consumidas en una ocasión o porciones de consumo habitual, establecidas en las siguientes tablas (5 y 6). Se aceptará una tolerancia de - 30% o +30% de la cantidad de referencia, si el fabricante excede el 30% deberá calcular el número de porciones por envase en el producto.
Tabla 5. Cantidades de Referencia para Alimentos menores de 4 años
| Alimento | Cantidad de referencia |
| Cereales secos instantáneos para preparar colada | 10 g |
| Cereales secos instantáneos para preparar papilla | 20 g |
| Galletas | 10 g |
| Compotas | 60 g |
| Leche (a partir de 1 año) | 80 mL |
| Yogurt | 60 g |
Tabla 6. Cantidades de Referencia para Alimentos en General (mayores de 4 años)
| Alimento | Cantidad de referencia |
| Almidón de maíz, papa, yuca | 10 g |
| Arroz crudo | 50 g |
| Avena en hojuela1 | 24 g |
| Harina de avena | 25 g |
| Harinas de trigo | 25 g |
| Harina de maíz | 25 g |
| Pasta para sopa1 | 15 g |
| Granos simples, por ejemplo cebada1 | 45 g |
| Harina como ingrediente principal1 | 50 g |
| Harina como ingrediente secundario1 | 20 g |
| Masa para empanadas, pasteles y panqueques | 30 g |
| Masa de pizza | 40 g |
| Pan corriente | 50 g |
| Pan de molde blanco | 22 g |
| Pan de molde integral | 32 g |
| Tostadas | 30 g |
| Tofu | 40 g |
| Cubitos de pan/crotones | 7 g |
| Galleta salada tipo Cracker | 24 g |
| Pan Francés | 35 g |
| Alimento | Cantidad de referencia |
| Miga de pan | 30 g |
| Pastas cortas y largas crudas (como plato único)1 | 64 g |
| Pastas frescas con o sin relleno (por ejemplo: raviolis, tortellini) | 100 g |
| Pastas deshidratadas con relleno | 70 g |
| Lasagna preparada | 140 g |
| Lasagna seca | 55 g |
| Sémola como ingrediente principal1 | 70 g |
| Sémola como ingrediente secundario1 | 15 g |
| Trigo para kibe y proteína de soja texturizada | 50 g |
| Tortillas de maíz o trigo/tacos | 30 g |
| Waffles | 85 g |
| PRODUCTOS DE PASTELERÍA | |
| Barras de cereal | 30 g |
| Brownies y alfajores | 40 g |
| Donas, muffins | 55 g |
| Galletas | 30 g |
| Pasteles/Tortas de frutas, vegetales, queso o similares | 125 g |
| Pastelillo | 50 g |
| Rellenos o cubiertas para tortas | 35 g |
| Tartaleta | 80 g |
| Tortas preparadas sin relleno o con relleno | 60 g |
| Productos de pastelería, salados o dulces sin relleno | 40 g |
| Mezcla pastelera | 30 g |
| Polvo de hornear | 0.6 g |
| CEREALES PARA DESAYUNO | |
| Mezcla para preparar bebida a base de cereal, listo para reconstituir (tipo refresco instantáneo) | Cantidad necesaria para preparar un vaso de 200 mL |
| Cereales para desayuno (tipo cereal caliente), hojuelas de maíz | 40 g seco; 55 g con sabor y endulzado |
| Cereales para desayuno (tipo cereal caliente) hojuelas de avena | 1 taza preparada con 22 g de cereal seco simple |
| Cereales para desayuno, listo para consumir. | 30 g |
| Cereales para desayuno, listo para consumir, pesando menos de 20 g por taza; por ejemplo, granos de cereal simple expandido | 15 g |
| Salvado de avena | 21 g |
| Salvado o germen de trigo | 10 g |
| Hojuelas de trigo o maíz | 30 g |
| PAPAS | |
| Papas a la francesa prefritas congeladas | 80 g |
| Papa fresca o congelada | 80 g |
| VEGETALES SIN SALSA FRESCOS O CONGELADOS | |
| Vegetales frescos o congelados3 | 85 g |
| Ají, cebolla3 | 30 g |
| OTROS VEGETALES | |
| Vegetales usados principalmente para aderezar (por ejemplo: pimentón, perejil)1 | 4 g |
| Todos los vegetales sin salsa enlatados en líquido | 130 g |
| Vegetales en conserva [alcachof, espárrago, hongos, ajíes, pepino y palmitos] en salmuera, vinagre y aceites. | 50 g |
| Vegetales deshidratados en conserva (tomate seco) | 40 g |
| Jugo de vegetales | 200 mL |
| Alimento | Cantidad de referencia |
| Aceitunas, alcaparras 2 | 15 g |
| Encurtidos, todos los tipos2 | 30 g |
| Pasta de vegetales (por ejemplo: pasta de tomate) | 30 g |
| Salsa de vegetales (por ejemplo: salsa de tomate) | 15 g |
| PLATOS PREPARADOS CONGELADOS | |
| Plato mixto (carne o pollo con agregado) | 250 g |
| Plato mixto de vegetal | 135 g |
| OTROS PLATOS PREPARADOS | |
| Medibles en tazas (por ejemplo: espagueti con salsa, etc.) | 1 taza |
| No medibles en taza (por ejemplo: burritos, pizza, sándwiches, etc.) | 140 g (adicionar 55 g para productos que llevan algún tipo de salsa) |
| FRUTAS PROCESADAS | |
| Todas las frutas enlatadas o congeladas, coctel de frutas, excepto las listadas en categorías separadas | 140 g |
| Ciruelas deshidratadas (secas) | 40 g |
| Durazno deshidratado (seco) | 60 g |
| Brevas en almibar | 100 g |
| Uvas pasas | 30 g |
| Duraznos mitades2 | 85 g |
| Duraznos trozados2 | 85 g |
| Frambuesas1 | 85 g |
| Frutas para adorno o sabor (por ejemplo: cerezas) | 20 g |
| Frutas para aderezar (por ejemplo: salsa o puré de ciruela) | 70 g |
| Otras frutas usadas como ingrediente principal | 55 g |
| Jugos, néctares y bebidas de fruta | 200 mL |
| Jugos usados como ingredientes (por ejemplo: jugo de limón) | 5 mL |
| Frutas en almíbar o encurtidas2 | 30 g |
| Salsa a base de frutas (por ejemplo: salsa de frambuesa, salsa de fresa) | 30 g |
| PRODUCTOS LÁCTEOS | |
| Arequipe/Manjar blanco | 30 g |
| Crema chantillí | 10 g |
| Crema de leche | 15 g |
| Suero para untar | 30 g |
| Helados | 45 g (1 bola pequeña) |
| Helados en porción individual (por ejemplo: paletas, vasito, cono, sándwich de helado, etc.) | 1 unidad |
| Kumis | 150 mL / g |
| Yogurt cremoso | 150 g |
| Yogurt líquido | 200 mL |
| Bebidas lácteas fermentadas | 200 mL |
| Leche condensada | 20 g |
| Leche evaporada | 30 g |
| Leche en polvo | Cantidad necesaria para preparar un vaso 200 mL (sin hielo) |
| Leche líquida | 200 mL |
| Bebidas con leche | 200 mL |
| Quesillo | 30 g |
| Queso cottage | 110 g |
| Queso fresco o campesino | 30 g |
| Queso para untar | 15 g |
| Alimento | Cantidad de referencia |
| Queso rallado | 18 g |
| Quesos excepto los listados en categorías separadas | 30 g |
| Queso tipo petit suisse | 30 g |
| Postre lácteo | 80 g |
| Postre lácteo con fruta | 145 g |
| PRODUCTOS DE LA PESCA, CARNES Y SUS DERIVADOS | |
| Anchoas enlatadas | 15 g |
| Caviar | 10 g |
| Carnes embutidas | 50 g |
| Albondigas a base de carne | 80 g |
| Chorizo y Longaniza | 50 g |
| Jamón Tajado y Mortadela | 30 g |
| Salchicha | 40 g |
| Hamburguesa | 70 g |
| Paté | 15 g |
| Tocineta | 10 g |
| Pescados, mariscos ahumados | 55 g |
| Conserva de pescado (por ejemplo: salmón, jurel u otro) | 100 g |
| Pescados (atún, sardinas), mariscos enlatados2 | 60 g |
| Patés (jamón, hígado, panceta, etcétera) | 10 g |
| HUEVO | |
| Huevo fresco1 | 50 g |
| Ovoproductos (huevo en polvo) | Cantidad para reemplazar un huevo de 50 g |
| LEGUMINOSAS EN GRANO SECO | |
| Arveja, garbanzos, lentejas, fríjol, habas1 | 60 g |
| LEGUMINOSAS ENLATADAS | |
| Arveja, garbanzos, lentejas, fríjol | 120 g |
| ACEITES Y GRASAS | |
| Aceites | 10 mL |
| Mantequilla | 7 g |
| Sustitutos de mantequilla, en polvo | 2 g |
| Margarina | 10 g |
| Mayonesa | 12 g |
| Aceite en aerosol (tipo spray) | 0.25 g |
| NUECES Y SEMILLAS | |
| Coco rallado | 15 g |
| Nueces | 30 g |
| Maní | 30 g |
| Almendras | 30 g |
| Mezclas de ellos | 30 g |
| Pastas y cremas de nueces (por ejemplo: pasta de maní) | 2 cucharadas – 20 g |
| Semillas oleaginosas (mezcladas, cortadas, picadas, entereas) | 15 g |
| AZÚCAR, PRODUCTOS DE CHOCOLATE Y OTROS PRODUCTOS DULCES | |
| Arequipe, manjar | 20 g |
| Azúcar | 5 g |
| Sustitutos de azúcar | Cantidad equivalente a la cantidad de referencia de azúcar para endulzar |
| Jarabe de maíz, miel, cobertura de frutas, y otros jarabes (cassis, grosella, frambuesa, mora, guaraná, etcétera). | 20 g |
| Bebidas carbonatadas | 200 mL |
| Alimento | Cantidad de referencia |
| Bebidas no carbonatadas | 200 mL |
| Bebidas hidratantes | 200 mL |
| Bebidas hidratantes en polvo | 20 g – 30 g |
| Caramelos, dulces4 | 20 g |
| Mezcla para preparar bebida lista para reconstituir (tipo refresco instantáneo) | Cantidad necesaria para preparar un vaso de 200 mL |
| Dulces de corte (guayaba, membrillo, higo, batata, etcétera). | 40 g |
| Goma de mascar (chicle)4 | 3 g |
| Masmelos | 30 g |
| Mermelada | 20 g |
| Miel de abejas | 10 g |
| Miel para pancakes | 10 g |
| Salsa de chocolate | 30 g |
| Chocolate de consumo directo | 25 g |
| Chocolate de mesa sin azúcar | 8 g |
| Chocolate de mesa con azúcar | 20 g |
| Polvo achocolatado, polvos a base de cacao, chocolate en polvo y cacao en polvo. | 20 g |
| Panela | 25 g |
| Decorativos para productos horneados, tortas, galletas (por ejemplo: azúcar de color, chispas de chocolate). | 1 cucharadita o 4 g si no se puede medir en cucharaditas |
| MISCELÁNEOS | |
| Café soluble | Cantidad necesaria para preparar una taza |
| Café molido | Cantidad necesaria para preparar una taza |
| Achiras | 25 g |
| Extruidos de maíz | 15 g |
| Tortillas de maíz | 30 g |
| Mixtos (papa-tajada-chicharrón) | 40 g |
| Maíz pira | 25 g |
| Productos para snacks o botanas a base de cereales, harinas, tubérculos, raíces y otros, extruidos o no | 25 g |
| Productos expandidos o de pellet de harina/ chicharrón | 15 g |
| Paleta de agua, congelados con sabor y endulzados | 85 g |
| Mezclas en polvo para preparar bebidas (sin alcohol) | Cantidad necesaria para preparar 1 vaso (sin hielo) |
| Mezclas secas para recubrir carne, pescados, mezclas sazonantes | 12 g |
| Especias, hierbas, (diferentes a los suplementos dietarios) | ¼ de cucharadita o 0.5 g si no es medible en cucharaditas |
| Salsas para pasta | 125 g |
| Salsa inglesa, salsa de soya, salsa para carnes | 5 mL |
| Salsa tártara | 15 g |
| Salsas picantes | 6 g |
| Aderezo para ensaladas | 30 g |
| Mostaza | 10 g |
| Vinagre | 5 mL |
| Vino de cocina | 5 mL |
| PRODUCTOS DESHIDRATADOS | |
| Caldos deshidratados y concentrados | 3 g o Cantidad suficiente para preparar 250 ml |
| Condimentos preparados, incluidos los deshidratados (Ejemplo: chille seco, ají panka, merken, etc.) | 5 g |
| Alimento | Cantidad de referencia |
| Sazonadores y mezclas deshidratadas típicas de cada país para preparaciones varias. Incluye sazonador Umami | 3 g |
| Cremas en polvo y sopas deshidratadas | 20 g o Cantidad suficiente para preparar 250 ml |
Notas aclaratorias de la tabla con superíndices 1, 2, 3 y 4
1. Las cantidades de referencia se refieren a los alimentos tal como se comercializan, como por ejemplo productos crudos o procesados (cereales, leguminosas, etc.).
2. Para alimentos empacados con un líquido, la cantidad de referencia se refiere a los sólidos drenados, excepto para alimentos en los que tanto sólidos como líquidos son consumidos.
3. Cantidades de referencia para alimentos listos para el consumo, o casi listos para el consumo (por ejemplo, calentar y servir o dorar y servir).
4. El tamaño de porción en la etiqueta para todos los caramelos, dulces y las gomas de mascar (chicle) con un peso diferente al de la cantidad de referencia, será considerado una porción, siempre y cuando cumpla con la definición establecida en el presente acto administrativo.
PARÁGRAFO 1o. Si el contenido completo del envase vendido individualmente puede ser razonablemente consumido en una ocasión o es una porción de consumo habitual, puede ser etiquetado como una (1) sola porción.
PARÁGRAFO 2o. Para los alimentos que no se encuentran definidos en las tablas de este anexo, será responsabilidad del fabricante establecer el tamaño de la porción que declare en la etiqueta y su equivalencia con respecto a medidas caseras y unidades del sistema internacional. En estos casos la porción debe cumplir con la definición establecida en el presente acto administrativo.
12.2 Se requiere que los productores de alimentos hagan la conversión de la cantidad de referencia al tamaño de porción en la etiqueta en una medida casera apropiada para su producto específico, usando los procedimientos establecidos en el Capítulo II del presente reglamento.
12.3 Las medidas caseras comunes constituyen la base obligatoria para las declaraciones del tamaño de las porciones e incluyen: la taza; el vaso; la cucharada; la cucharadita; la rebanada o tajada; la fracción de la unidad; los recipientes comúnmente usados en la casa como la jarra, bandeja u otra medida casera común para envasar alimentos. No obstante, en aquellos alimentos en los que no sea posible expresar una porción en estas medidas, se podrá utilizar como medida casera una rebanada, una fracción de la unidad, onzas o el número de unidades que más se aproxime a la cantidad de referencia.
12.4 La declaración del tamaño de la porción debe expresar en medidas caseras y entre paréntesis la cantidad en unidades de acuerdo al Sistema Internacional de Unidades (valor de la magnitud con su respectiva unidad).
a) Los líquidos deben ser declarados usando mililitros (mL) y cualquier otro alimento en gramos (g). Los gramos deben ser aproximados al número entero más cercano, con excepción de cantidades menores de 5 g. Para cantidades entre 2 g y 5 g los números se deben aproximar al 0.5 g más cercano y cantidades menores de 2 g deben ser aproximadas al 0.1 g más cercano.
b) El tamaño de las porciones puede ser declarado también en onzas (oz) y onzas fluidas (oz fl), en paréntesis, después de la medida del sistema internacional de unidades, separada por una línea diagonal, cuando otras medidas caseras comunes constituyen la declaración principal para la porción del alimento.
12.5 Declaración de las medidas caseras: Las medidas caseras deben expresarse de la siguiente forma:
a) Taza: Se expresa en incrementos de 1/4 o 1/3 de taza;
b) Cucharada: Se expresa como 1, 1 1/3, 1 1/2, 1 2/3, 2, o 3 cucharadas;
c) Cucharadita: Se expresa como 1/8, 1/4, 1/2, 3/4, 1, o 2 cucharaditas.
12.6 Número de porciones por envase: si un envase contiene más de una porción, el fabricante debe hacer el cálculo con base en la cantidad de referencia definida en las tablas 5 y 6. El número de porciones que se declare en el rótulo o etiqueta puede ser expresado con el número entero más cercano y utilizar la palabra “aproximadamente” o su abreviación “aprox”. No obstante, se aceptan las siguientes excepciones:
a) Los envases que contienen entre 1 y 5 porciones pueden expresarlas con el número más cercano a 0.5 de la porción y la palabra “aproximadamente”. Por ejemplo: aproximadamente 3.5 porciones.
b) Cuando la porción es calculada con base en los sólidos drenados y el número de porciones cambia debido a la variación natural del tamaño de la unidad (pepinillos encurtidos, entre otros), se puede declarar el número usual de porciones en un envase. Por ejemplo, “usualmente 5 porciones”.
12.7 Porciones de alimentos en unidades individuales (por ejemplo: galletas, panecillos, pan tajado, ponqué tajado): el tamaño de la porción será determinado de acuerdo con los tamaños establecidos en las tablas 5 y 6 y una tolerancia de - 30% o +30% del valor de referencia.
PARÁGRAFO. Se exceptúan del anterior criterio, los alimentos con variación natural de tamaños, tales como frutas en almíbar tipo conserva (cerezas marrasquino, brevas, duraznos), vegetales en medio líquido, productos en escabeche y otros productos similares, en los cuales se debe declarar el tamaño de una (1) porción en peso que más se aproxime a la cantidad de referencia correspondiente.
12.8 Porciones de alimentos en unidades grandes normalmente divididos para su consumo (Ejemplos: tortas, pasteles, pizza): El tamaño de una porción es la rebanada o tajada, expresada como una fracción del total más cercana a la cantidad de referencia. Las rebanadas se pueden expresar como 1/2, 1/3, 1/4, 1/5, 1/6, o fracciones más pequeñas que se pueden expresar dividiendo estos valores por 2 o 3. Se permite usar 1/8, 1/12 y 1/16 pero no las fracciones 1/7, 1/11, 1/13 y 1/14.
12.9 Porciones de alimentos en presentaciones no contempladas en el numeral 12.1 (Ejemplos: harina, salsas en general, esparcibles), y comidas, bebidas y platos preparados listos para consumo y para servir directamente al público y comidas y platos preparados que necesariamente requieren cocción:
a) El tamaño de una porción es la cantidad expresada en medidas caseras que más se aproxime a la cantidad de referencia del alimento;
b) Para comidas, bebidas y platos preparados listos para consumo y para servir directamente al público y comidas y platos preparados que necesariamente requieren cocción, envasados o empacados en porciones individuales y cumpliendo con las disposiciones para porciones individuales, el tamaño de su porción, será el contenido comestible íntegro del envase.
12.10 Envases de alimentos surtidos: para productos que contienen un surtido de porciones individuales o dos o más compartimentos, con un alimento diferente en cada compartimiento, deben incluir el rotulado o etiquetado nutricional para cada variedad de alimento, por tamaño de porción y por 100 g o mL, calculados con base en la cantidad de referencia correspondiente. Lo anterior no aplica para envases de alimentos surtidos en los que puede leerse la información nutricional de los productos que lo contienen a través de su empaque.
ARTÍCULO 13. EQUIVALENCIAS DE LAS MEDIDAS CASERAS COMUNES. Para la declaración del tamaño de las porciones se establecen las siguientes equivalencias con el sistema internacional de unidades:
1 cucharadita (cdta) equivale 5 mL
1 cucharada (cda) equivale 15 mL
1 taza equivale a 200 mL o 240 mL
1 vaso equivale a 200 mL o 240 mL
1 onza fluida (oz fl) = 30 mL
1 onza de peso (oz) = 28 g
PARÁGRAFO 1o. Se exceptúan estas medidas para los alimentos que incluyen su propia unidad de medida incluida en el empaque.
PARÁGRAFO 2o. Para productos secos tener en cuenta la densidad para hacer la respectiva relación.
ARTÍCULO 14. ABREVIATURAS PERMITIDAS. Para la declaración de energía, nutrientes y el tamaño de las porciones de que trata el presente capítulo, únicamente se permite el uso de las siguientes abreviaturas:
Tabla 7. Abreviaturas permitidas en nutrientes
| Nutrientes | Abreviatura permitida |
| Grasa total | Grasa |
| Grasa saturada/Ácidos grasos saturados | Grasa sat. |
| Grasa poliinsaturada | Grasa poliinsat. |
| Grasa monoinsaturada | Grasa monoinsat. |
| Grasa Trans/Ácidos Grasos Trans | Trans |
| Carbohidratos Totales | Carb. Total |
| Azúcares añadidos | Az. Añadidos |
| Fibra dietaria | Fibra |
| Vitamina | Vit. |
Tabla 8. Abreviaturas permitidas en tamaños de porciones
| Tamaño de las porciones | Abreviatura permitida |
| Cucharadita | Cdta |
| Cucharada | Cda |
| Onza fluida | Oz fl |
| Onza | Oz |
| Gramos | g |
| Mililitro | mL |
| Tamaño de las porciones | Abreviatura permitida |
| Tamaño de la porción | Porción |
| Porciones por envase | Porciones |
| Aproximadamente | Aprox. |
VALORES DIARIOS DE REFERENCIA DE NUTRIENTES.
ARTÍCULO 15. VALORES DIARIOS DE REFERENCIA DE NUTRIENTES. Para el cumplimiento del etiquetado nutricional en los alimentos, se establecen los siguientes valores diarios de referencia de nutrientes, para niños mayores de 6 meses y menores de cuatro (4) años de edad y niños mayores de cuatro (4) años y adultos.
Tabla 9. Valores diarios de referencia de nutrientes - necesidades (VRN-N)
| Energía/Nutrientes | Unidad de Medida | Niños mayores de 6 meses y menores de 4 años | Niños mayores de 4 años y adultos |
| Energía /Calorías | Kcal | 1000 kcal | 2 000 kcal |
| Grasa total | Gramos | 33 g | 66 g |
| Grasa monoinsaturada | Gramos | NE | NE |
| Grasa poliinsaturada | Gramos | NE | NE |
| Carbohidratos totales | Gramos | 150 g | 300 g |
| Fibra dietaria | Gramos | 14 g | 28 g |
| Proteínas | Gramos | 25 g | 50 g |
| Vitamina A | íg ER | 300 íg ER | 800 íg ER |
| Vitamina C/ Ácido Ascórbico | Miligramos | 15 mg | 83 mg |
| Calcio | Miligramos | 700 mg | 1 000 mg |
| Hierro | Miligramos | 11 mg | 20 mg |
| Vitamina D | microgramos/Unidades Internacionales | 15 íg / 600 UI | 15 íg / 600 UI |
| Vitamina E | Miligramos ET | 5 mg | 9 mg |
| Vitamina B1/Tiamina | Miligramos | 0.5 mg | 1.15 mg |
| Vitamina B2/Riboflavina | Miligramos | 0.5 mg | 1.2 mg |
| Niacina/Ácido nicotínico | Miligramos | 6 mg | 15 mg |
| Vitamina B6/Piridoxina | Miligramos | 0.5 mg | 1.3 mg |
| Ácido Fólico /Folacín/ Folato | Microgramos | 150 íg | 400 íg |
| Vitamina B12/Cobalamina | Microgramos | 0.9 íg | 2.4 íg |
| Fósforo | Miligramos | 460 mg | 700 mg |
| Yodo | Microgramos | 90 íg | 150 íg |
| Magnesio | Miligramos | 80 mg | 310 mg |
| Zinc | Miligramos | 3 mg | 11 mg |
| Cobre | Microgramos | 340 íg | 900 íg |
| Ácido Pantoténico | Miligramos | 2 mg | 5 mg |
| Vitamina K | Microgramos | 25 íg | 65 íg |
| Selenio | Microgramos | 20 íg | 70 íg |
| Potasio | Miligramos | 3000 mg | 4700 mg |
NE: No Especificado para etiquetado nutricional.
ER: Equivalente de retinol
ET: Equivalente de á-tocoferol
Tabla 10. Valores de referencia de nutrientes - enfermedades no transmisibles
(VRN-ENT)
| Nutrientes | Unidad de Medida | Niños mayores de 7 meses y menores de 4 años | Niños mayores de 4 años y adultos |
| Sodio, Máx. | Miligramos | 1000 mg | 2000 mg |
| Grasa saturada, Máx. | Gramos | NE | 20 g |
| Grasa trans, Máx. | Miligramos | NE | 2200 mg |
| Azúcares añadidos, Máx. | Gramos | 25 g | 50 g |
| Colesterol, Máx. | Miligramos | NE | 300 mg |
NE: No Especificado para etiquetado nutricional.
PARÁGRAFO 1o. Para el caso de la Vitamina A, 1 ER es = 1 íg de Retinol o 6 íg de â-caroteno o 12 íg de otros carotenoides. Cuando se dispone del contenido de carotenoides provitamina A (á-caroteno, â-caroteno, â-criptoxantina) en los alimentos se deben utilizar los íg de Actividad Equivalente de Retinol (íg RAE). 1 íg RAE = 1 íg de Retinol o 12 íg de â-caroteno o 24 íg de á-caroteno y â criptoxantina.
PARÁGRAFO 2o. Para el caso de Folato, 1 EFD = 1 íg de folato dietético = 0,6 íg de ácido fólico adicionado a los alimentos o como suplemento ingerido con las comidas = 0,5 íg de ácido fólico de suplementos ingerido con el estómago vacío.
DECLARACIÓN DE PROPIEDADES NUTRICIONALES.
ARTÍCULO 16. REQUISITOS GENERALES. <Artículo modificado por el artículo 3 de la Resolución 2492 de 2022. El nuevo texto es el siguiente:> Todo alimento que haga uso de declaraciones de propiedades nutricionales debe cumplir con los siguientes requisitos:
16.1. Las únicas declaraciones de propiedades nutricionales permitidas serán las que se realicen con base en los valores diarios de referencia establecidos en el presente reglamento técnico, y a los ácidos grasos establecidos en los artículos 19.1 y 19.2 del mismo reglamento técnico.
16.2. El tamaño de letra de los términos o descriptores utilizados para las declaraciones de propiedades nutricionales no podrá exceder más de dos veces el tamaño de las letras usadas en el nombre del alimento.
16.3. Cuando un producto cuente con 1 o más sellos frontales de advertencia, no podrá realizar declaraciones de propiedad nutricionales.
PARÁGRAFO. Las declaraciones de propiedades nutricionales que ya habían sido aprobadas por la Sala Especializada de Alimentos y Bebidas del Invima seguirán estando vigentes, para el presente reglamento técnico. Adicionalmente, si se requiere de otra declaración de un nutriente que no tenga valor de referencia, el fabricante deberá solicitarlo a esa entidad
ARTÍCULO 17. TIPOS DE DECLARACIONES DE PROPIEDADES NUTRICIONALES. Las declaraciones de propiedades nutricionales son:
17.1 Declaración de propiedades relativas al contenido de nutrientes: se entiende por declaración de propiedades nutritivas que describe el nivel de un determinado nutriente contenido en un alimento. (Ejemplos: “Fuente de calcio”; “excelente contenido de fibra y bajo de grasa”; “fortificado”).
17.2 Declaración de propiedades de comparación de nutrientes: se entiende una declaración de propiedades que compara los niveles de nutrientes y/o el valor energético de dos o más alimentos. (Ejemplos: “reducido”; “menos que”; “menos”; “más que”; “aumentado”; “más”; “doble”).
17.3 Declaración de propiedades de no adición: se entiende cualquier declaración de propiedades de que no se ha añadido un ingrediente a un alimento, sea directa o indirectamente. El ingrediente es uno cuya presencia o adición está permitida en el alimento y que los consumidores esperarían normalmente encontrar en el alimento. Por ejemplo “sin azúcar añadido” en una galleta.
ARTÍCULO 18. CONDICIONES GENERALES PARA LA DECLARACIÓN DE PROPIEDADES RELACIONADAS CON EL CONTENIDO DE NUTRIENTES. Las condiciones generales para la declaración de propiedades relacionadas con el contenido de nutrientes son las siguientes:
18.1 La declaración debe utilizar los términos o descriptores que se ajusten al contenido del nutriente, fibra dietaria o energía del alimento. No se podrá utilizar términos, descriptores o sinónimos diferentes a los permitidos en el presente reglamento.
18.2 El término “libre de sal” debe cumplir con el criterio “libre de sodio” y los criterios de “Sin sal/sodio añadido”.
18.3 Para los efectos de las declaraciones de propiedades nutricionales, se entenderá que un alimento es sólido o líquido según la unidad de medida utilizada en la declaración del contenido neto del alimento, es decir, será sólido si su contenido neto está expresado en gramos u otra medida equivalente, o líquido si su contenido neto está expresado en mililitros u otra medida equivalente. En los productos destinados a ser reconstituidos o que requieran preparación antes de ser consumidos, la declaración nutricional debe realizarse de acuerdo con las instrucciones recomendadas por el fabricante en la etiqueta.
ARTÍCULO 19. TÉRMINOS O DESCRIPTORES PERMITIDOS PARA LAS DECLARACIONES DE PROPIEDADES RELACIONADAS CON EL CONTENIDO DE NUTRIENTES. Excelente fuente, Buena fuente, Libre de, Bajo, Muy bajo, Magro, Extramagro, Fortificado.
19.1 Excelente fuente: deben cumplir con los siguientes requisitos:
Tabla 11. Condiciones para el descriptor “Excelente fuente”:
| Componente | Condiciones: no menos de |
| Proteína | 20% de VRN por 100 g (sólidos) 10% de VRN por 100 mL (líquidos) o 20% de VRN por porción de alimento. |
| Vitaminas y minerales | 30% de VRN por 100 g (sólidos) 15% de VRN por 100 mL (líquidos) o o 30% de VRN por porción de alimento. |
| Fibra | 6 g por 100 g o mL o 20% del valor diario de referencia por porción. |
| Ácidos grasos omega-3 | 0.6 g de ácido alfa-linolénico o al menos 80 mg de la suma de ácido eicosapentanoico y ácido decosahexanoico. Por 100 g o 100 mL. |
| Grasas monoinsaturadas | Al menos un 45% de los ácidos grasos presentes en el alimento proceden de grasas monoinsaturadas y las grasas monoinsaturadas aportan más del 20% del valor energético del producto. |
| Grasas poliinsaturadas | Al menos un 45% de los ácidos grasos presentes en el alimento proceden de grasas poliinsaturadas y las grasas poliinsaturadas aportan más del 20% del valor energético del producto. |
| Componente | Condiciones: no menos de |
| Grasas insaturadas | Al menos un 70% de los ácidos grasos presentes en el alimento proceden de grasas insaturadas y las grasas insaturadas aportan más del 20% del valor energético del producto. |
PARÁGRAFO 1o. Los alimentos que cumplan con el descriptor “excelente fuente de”, también podrán utilizar el siguiente sinónimo: “rico en”.
PARÁGRAFO 2o. Cuando el alimento cumpla con el descriptor “excelente fuente “para 3 o más vitaminas y/o minerales podrá utilizar el descriptor “excelente fuente de vitaminas y/o minerales”.
19.2 Buena fuente: deben cumplir con los siguientes requisitos:
Tabla 12. Condiciones para el descriptor “Buena fuente”:
| Componente | Condiciones: no menos de |
| Proteína | 10 % de VRN por 100 g (sólidos) 5 % de VRN por 100 mL (líquidos) o 10 % de VRN por porción de alimento |
| Vitaminas y minerales | 15 % de VRN por 100 g (sólidos) 7.5 % de VRN por 100 mL (líquidos) o 15% de VRN por porción de alimento |
| Fibra | 3 g por 100 g o mL o 10% del valor diario de referencia por porción |
| Ácidos grasos omega-3 | Al menos 0.3 g de ácido alfa-linolénico, o al menos 40 mg de la suma de ácido eicosapentaenoico y ácido decosahexaenoico. Por 100 g o 100mL |
PARÁGRAFO 1o. Los alimentos que cumplan con el descriptor “buena fuente”, también podrán utilizar los siguientes sinónimos: “proporciona”, “fuente”, “contiene” o “con”.
PARÁGRAFO 2o. Cuando el alimento naturalmente tiene algún nutriente en una cantidad suficiente para declarar este descriptor, puede utilizarse el término “naturalmente con”.
PARÁGRAFO 3o. Cuando el alimento cumpla con el descriptor “buena fuente de” para 3 o más vitaminas y/o minerales podrá utilizar el descriptor “buena fuente de vitaminas y/o minerales
19.3 Libre de: para utilizar el descriptor “libre de” los alimentos deben cumplir los siguientes requisitos:
Tabla 13 Requisitos para el descriptor “Libre de”
| Nutriente | Requisitos para el descriptor “Libre de” (por 100 g para alimentos sólidos o 100 mL para alimentos líquidos) |
| Calorías: | – Contiene no más de 4 kcal (únicamente para líquidos). – Si un alimento cumple con esta condición sin necesidad de procesamiento o alteración especial, formulación o reformulación para disminuir el contenido calórico, la etiqueta debe incluir una declaración indicando que, el alimento naturalmente, es libre de calorías; |
| Grasa: | – Contiene no más de 0.5 g de grasa total. – El alimento no debe contener ingredientes que sean grasas, que puedan ser interpretados por el consumidor como que contienen grasa. – Si el alimento cumple con las anteriores condiciones sin necesidad de procesamiento o alteración especial, formulación o reformulación para disminuir el contenido de grasa, la etiqueta debe incluir una declaración indicando que el alimento naturalmente es libre de grasa. El término “libre de grasa” podrá ser utilizado en la leche descremada, siempre y cuando cumpla los requisitos establecidos en este literal. |
| Grasa saturada | – Contiene no más de 0.1 g de grasa saturada. – El alimento no debe contener ingredientes que sean grasas, que puedan ser interpretados por el consumidor como que contienen grasa. – Si el alimento cumple con las anteriores condiciones sin necesidad de procesamiento o alteración especial, formulación o reformulación para disminuir el contenido de grasa saturada, la etiqueta debe incluir una declaración indicando que el alimento naturalmente es libre de grasa saturada. |
| Ácidos grasos trans: | – Contiene no más de 100 mg de grasas trans. – El alimento no debe contener ingredientes que sean grasas, que puedan ser interpretados por el consumidor como que contienen grasa. – Si el alimento cumple con las anteriores condiciones sin necesidad de procesamiento o alteración especial, formulación o reformulación para disminuir el contenido de ácidos grasos trans, la etiqueta debe incluir una declaración indicando que el alimento, naturalmente es libre de grasa trans. |
| Azúcares totales | – Contiene no más de 0.5 g de azúcares. |
| Colesterol | – Contiene menos de 5 mg por 100 g (sólidos) o por 100 mL (líquidos) y, para ambas declaraciones menos de: 1,5 g de grasa saturada por 100 g (sólidos), 0.75 g de grasa saturada por 100 mL (líquidos) y menos de 10 % de energía de grasa saturada. – Si el alimento cumple con las anteriores condiciones sin necesidad de procesamiento o alteración especial, formulación o reformulación para disminuir el contenido de colesterol, la etiqueta debe incluir una declaración indicando que el alimento, naturalmente es libre de colesterol. |
| Sodio: | – Contiene no más de 5 mg de sodio. – El alimento no debe contener cloruro de sodio o cualquier otro ingrediente o aditivo que contenga sodio. – Si el alimento cumple con las anteriores condiciones sin necesidad de procesamiento o alteración especial, formulación o reformulación para disminuir el contenido de sodio, la etiqueta debe incluir una declaración indicando que el alimento naturalmente es libre de sodio. |
19.3.1 Los alimentos que cumplan con el descriptor “libre de”, también podrán utilizar los siguientes sinónimos: “no contiene”; “no tiene” “cero” (o su expresión numérica); “exento de” o “fuente no significativa de” “sin”.
19.3.2 El uso de los términos “libre”, “bajo” implica que el alimento ha sido modificado en alguna manera, estos se podrán utilizar únicamente en alimentos que han sido especialmente procesados, modificados o formulados, con el fin de disminuir o remover una cantidad de un nutriente presente en el alimento. Por ejemplo: Las arvejas enlatadas habitualmente contienen sodio, en consecuencia, si este alimento es procesado de tal manera que cumple con los requisitos para ser considerado “bajo” o “libre” en sodio podrá denominarse de esta forma.
19.3.3 Cuando se trate de alimentos que, por su naturaleza, poseen un bajo contenido o están exentos del nutriente al que se refiere la declaración de propiedades, los términos utilizados para describir el nivel del nutriente no deben dar a entender que es una cualidad exclusiva de ese producto, sino que se trata de una cualidad natural del alimento.
19.4 Bajo en: para utilizar el descriptor “bajo en” los alimentos deben cumplir los siguientes requisitos:
Tabla 14. Requisitos para el descriptor “Bajo en”
| Nutriente | Requisitos para el descriptor “Bajo en” (por 100 g o 100 mL) |
| Calorías: | – Contiene un máximo de 40 kcal por 100 g o 20 kcal por 100 mL. |
| Grasa: | – Contiene un máximo de 3 g por 100 g (sólidos) o 1.5 g por 100 mL (líquidos). El término “bajo en grasa” podrá ser utilizado en la leche semidescremada, siempre y cuando cumpla los requisitos establecidos en este literal. |
| G r a s a saturada | – Contiene un máximo de 1.5 g por 100 g (sólidos), 0.75 g por 100 mL (líquidos) y no más del y 10 % de energía proviene de grasa saturada |
| Colesterol | – Contiene un máximo de 0.02 g por 100 g (sólidos) 0.01 g por 100 mL (líquidos) |
| Sodio: | – Contiene un máximo de 80 mg por 100 g o 100 mL de alimento. El término “bajo en sal” puede usarse si el producto cumple con el criterio “bajo en sodio”. |
PARÁGRAFO. Los alimentos que cumplan con el descriptor “bajo en”, también podrán utilizar los siguientes sinónimos: “poco”, “pocas”, “baja fuente de” o “contiene una pequeña cantidad de”, “bajo aporte” y “bajo contenido”.
19.5 Muy bajo en: solamente se permite para sodio, si contiene un máximo de 40 mg por 100 g o 100 mL de alimento.
19.6 Magro: solamente aplica para carnes y pescados, debe contener menos de 10 g de grasa total, menos de 4.5 g de grasa saturada y menos de 95 mg de colesterol por porción declarada en la etiqueta.
PARÁGRAFO. Para el caso de los quesos, se permite este descriptor cumpliendo con lo establecido en las Resoluciones número 2310 de 1986 y 1804 de 1989, o la norma que la modifique o sustituya.
19.7 Extramagro: solamente se aplica para carnes y pescados. Debe contener, máximo 5 g de grasa total, 2 g de grasa saturada y 95 mg de colesterol por porción declarada en la etiqueta.
19.8. Fortificado: para el uso de este descriptor, se deben cumplir los siguientes requisitos:
19.8.1 Principios generales para el uso del descriptor fortificado en los alimentos. La fortificación voluntaria de nutrientes esenciales a los alimentos cumplirá los siguientes principios generales:
a) Los nutrientes derivados de los alimentos incluidos en la dieta diaria deben ser considerados en concentraciones que no den lugar a una ingesta excesiva o insignificante del nutriente esencial fortificado, frente al que ya tiene.
b) La fortificación de un nutriente esencial no debe dar lugar a efectos perjudiciales en el metabolismo por interacción con ningún otro nutriente contenido en el alimento.
c) Las fuentes de los nutrientes esenciales pueden ser naturales o sintéticas, y su selección debe basarse en consideraciones como la seguridad y la biodisponibilidad. Además, los criterios de pureza deben tener en cuenta la normativa nacional o en su defecto las normas FAO/OMS, normas internacionales reconocidas y en ausencia de ésta, los libros de farmacopea internacionales.
d) El nutriente esencial deberá ser estable y disponible en el alimento bajo las condiciones usuales de envasado, procesamiento, almacenamiento y distribución.
e) El nutriente esencial debe ser biodisponible.
f) La fortificación de nutrientes esenciales a los alimentos no deberá utilizarse para inducir a error o a engaño al consumidor, en cuanto al valor nutricional del alimento.
g) Deberá disponerse de métodos de medición normalizados o internacionalmente aceptados por organismos competentes para control y/u observancia de las concentraciones de nutrientes esenciales fortificados en los alimentos.
19.8.2 Nutrientes esenciales que pueden adicionar para fortificar los alimentos. Los alimentos podrán fortificarse por uno o más de los nutrientes esenciales indicados a continuación, los compuestos vitamínicos y minerales deben ser los especificados en la siguiente tabla:
Tabla 15. Compuestos vitamínicos y/o minerales permitidos para fortificar
| Nutriente | Compuesto vitamínico y/o mineral |
| Vitamina A | - retinol - acetato de retinilo - palmitato de retinilo - beta-caroteno |
| Vitamina D | - colecalciferol - ergocalciferol |
| Vitamina E | - D-alfa-tocoferol - DL-alfa-tocoferol - acetato de D-alfa tocoferilo - acetato de DL-alfa tocoferilo - succinato ácido de D-alfa tocoferilo - Succinato de DL-alfa tocoferil polietilen glicol 1000 - ALFA-tocoferol < 20% - beta-tocoferol < 10% - gamma-tocoferol 50% – 70% - delta-tocoferol 10% – 30%. |
| Vitamina K | - filoquinona (fitomedianona) - menaquinona-7 y menaquinona-6 |
| Vitamina B1 | - clorhidrato de tiamina - mononitrato de tiamina - cloruro de monofosfato de tiamina - cloruro de pirofosfato de tiamina |
| Vitamina B2 | - riboflavina - riboflavina 5'-fosfato sódico |
| Niacina | - ácido nicotínico - nicotinamida - hexanicotinato de inositol (hexaniacinato de inositol) |
| Nutriente | Compuesto vitamínico y/o mineral |
| Ácido pantoténico | - D-pantotenato cálcico - D-pantotenato sódico - Dexpantenol - pantetina |
| Vitamina B6 | - clorhidrato de piridoxina - piridoxina 5'-fosfato - dipalmitato de piridoxina |
| Ácido fólico | - ácido pteroilmonoglutámico - L-metilfolato cálcico |
| Vitamina B12 | - Cianocobalamina - Hidroxocobalamina 5'-desoxiadenosilcobalamina - metilcobalamina |
| Vitamina C | - ácido L-ascórbico - L-ascorbato sódico - L-ascorbato cálcico - L-ascorbato potásico - 6-palmitato de L-ascorbilo - L-ascorbato de magnesio - L-ascorbato de zinc |
| Calcio | - carbonato de calcio - cloruro cálcico - sales cálcicas de ácido cítrico - gluconato cálcico - glicerofosfato de calcio - lactato de calcio - sales cálcicas de ácido ortofosfórico - hidróxido cálcico - malato de calcio - óxido de calcio - sulfato de calcio - citrato malato cálcico - acetato de calcio - L-ascorbato cálcico - bisglicinato de calcio - piruvato de calcio - succinato de calcio - L-lisinato de calcio - L-pidolato de calcio - L-treonato de calcio - Oligosacáridos fosforilados de calcio |
| Magnesio | - acetato de magnesio - carbonato de magnesio - cloruro de magnesio - sales magnésicas de ácido cítrico - gluconato de magnesio - glicerofosfato de magnesio - sales magnésicas de ácido ortofosfórico - lactato de magnesio - hidróxido de magnesio - óxido de magnesio - sulfato de magnesio - citrato de magnesio y potasio - L-ascorbato de magnesio - bisglicinato de magnesio - L-lisinato de magnesio - malato de magnesio - L-pidolato de magnesio - piruvato de magnesio - succinato de magnesio - taurinato de magnesio - acetil taurinato de magnesio - Carbonato ácido de magnesio |
| utriente | Compuesto vitamínico y/o mineral |
| Hierro | - carbonato ferroso - citrato ferroso - citrato férrico de amonio - gluconato ferroso - fumarato ferroso - difosfato férrico de sodio - lactato ferroso - sulfato ferroso - difosfato férrico (pirofosfato férrico) - fosfato ferroso amónico - sacarato férrico - hierro elemental (carbonilo + electrolítico + deshidrogenado) - bisglicinato de hierro - etilendiaminotetraacetato de ferrosódico (III) trihidratado - Succinato Ferroso - Pirofosfato de hierro - Ortofosfato férrico - Hierro elemental (carbonilo o electrolítico o deshidrogenado o reducido) |
| Cobre | - carbonato cúprico - citrato cúprico - gluconato cúprico - sulfato cúprico - complejo cobre-lisina - L-pidolato ferroso - fosfato ferroso - taurinato de hierro (II) |
| Cromo | - cloruro de cromo (III) - lactato de cromo (III) trihidrato - nitrato de cromo - picolinato de cromo - sulfato de cromo (III) - Nicotinato de cromo - Cromo aminoácido quelato - Cloruro de cromo hexahidratado - Polinicotinato de cromo |
| Zinc | - acetato de zinc - bisglicinato de zinc - cloruro de zinc - citrato de zinc - gluconato de zinc - lactato de zinc - óxido de zinc - carbonato de zinc - sulfato de zinc - L-ascorbato de cinc - L-aspartato de cinc - L-lisinato de cinc - malato de cinc - mono-L-metionina-sulfato de cinc - L-pidolato de cinc - picolinato de cinc - zinc metionina - zin histidina |
| Selenio | - selenito de sodio - selenito ácido de sodio - seleniato de sodio - levadura enriquecida con selenio* - Seleniometionina |
| Potasio | - bicarbonato de potasio - carbonato de potasio - cloruro de potasio - citrato de potasio - gluconato de potasio - glicerofosfato de potasio - lactato de potasio - hidróxido de potasio - sales potásicas de ácido ortofosfórico |
*Levadura enriquecida con selenio: levaduras producidas por cultivo en presencia de selenito de sodio como fuente de selenio y que contienen, en la forma seca comercializada, un máximo de 2.5 mg Se/g. La especie con selenio orgánico predominante presente en la levadura es seleniometionina (entre el 60% y el 85% del selenio extraído total presente en el producto). El contenido de otros compuestos orgánicos de selenio, incluida la selenocisteína, no excederá del 10% de selenio total extraído. Normalmente, los niveles de selenio inorgánico no superarán el 1% del selenio extraído total. Se consideran incluidos los diferentes grados de hidratación de los constituyentes.
PARÁGRAFO. Los compuestos vitamínicos o sales minerales no especificados en la Tabla 15, deberán ser aprobados por la Sala Especializada de Alimentos y Bebidas del Invima.
19.8.3 Rango del valor de referencia para el uso del descriptor “Fortificado”. Los alimentos que de manera voluntaria hagan el proceso de fortificación, deberán cumplir con el rango del 20% al 100% del VRN establecido en la Tabla 9 del presente reglamento, por porción declarada, sin superar para el grupo de menor edad al cual esté dirigido el producto, el Nivel de Ingesta Máximo Tolerable (UL), definido en la Resolución número 3803 de 2016, o la norma que la modifique o sustituya.
PARÁGRAFO 1o. Se excluyen del cumplimiento del presente artículo los alimentos cuya fortificación sea obligatoria. No obstante, si de forma voluntaria un fabricante hace una adición de micronutrientes adicional a la obligatoria, el alimento podrá declararse como fortificado.
PARÁGRAFO 2o. La declaración del descriptor “fortificado”, puede hacerse de la siguiente manera: “Fortificado con Vitaminas X y Minerales X”, “Más Vitaminas X y Minerales X”. La cual debe cumplir con los rangos establecidos, por porción declarada en la etiqueta. Cuando el alimento esté fortificado con más de tres (3) vitaminas y/o minerales, podrá utilizar la expresión “Fortificado con vitaminas y/o minerales”.
ARTÍCULO 20. CONDICIONES GENERALES PARA LA DECLARACIÓN DE PROPIEDADES NUTRICIONALES COMPARATIVAS. Las condiciones generales para la declaración de propiedades nutricionales comparativas son las siguientes:
20.1 La declaración de propiedades nutricionales comparativas, debe basarse en el alimento tal como se ofrece a la venta. En el caso de los alimentos envasados que deban prepararse o consumirse reconstituidos, se tendrá en cuenta la preparación posterior requerida para su consumo, de acuerdo con las instrucciones para su uso que se indican en la etiqueta.
20.2 Los alimentos comparados deben corresponder a versiones diferentes de un mismo alimento o alimentos similares y los alimentos que se comparan deben ser identificados claramente y en la misma porción o cantidad declarada.
20.3 Se debe indicar la cuantía de la diferencia en el valor energético o en el contenido de nutrientes de acuerdo con lo siguiente:
20.3.1 El valor de la diferencia expresado en porcentaje, en fracción o en una cantidad absoluta.
20.3.2 La identidad del alimento o alimentos con los cuales se compara el alimento en cuestión, de tal forma que el consumidor pueda identificarlos fácilmente.
20.3.3 La información indicada en los numerales 20.3.1 y 20.3.2 debe figurar junto o inmediatamente debajo del término descriptor utilizado para la declaración comparativa y en un tamaño de letra no menor de la mitad de dicho término.
20.4 El alimento reducido en grasa saturada, no debe aumentar el contenido de ácidos grasos trans.
20.5 El alimento reducido en ácidos grasos trans no debe aumentar el contenido de ácidos grasos saturados.
21.1 Reducido en: la comparación deberá basarse en una diferencia relativa de al menos 25 % en el valor energético o en el contenido de nutrientes respectivamente entre los alimentos comparados y una diferencia absoluta mínima por cada 100g para alimentos sólidos o semisólidos y por cada 100 mL para alimentos líquidos, tal como se muestra en la siguiente tabla:
Tabla 16. Requisitos para el descriptor “Reducido en”
| Nutriente | Diferencia relativa mínima | Diferencia absoluta mínima basada en 100 g o mL |
| Calorías | 25% | 40 kcal (Sólidos) |
| 20 kcal (Líquidos) | ||
| Grasas | 25% | 3 g (Sólidos) |
| 1.5 g (Líquidos) | ||
| Grasas Saturadas | 25% | 1.5 g (Sólidos) |
| 0.75 g (Líquidos) | ||
| Azúcares | 25% | 3 g (Sólidos) |
| 1.5 g (Líquidos) | ||
| Sodio | 25% | 80 mg |
| Colesterol | 25% | 20 mg (Sólidos) |
| 10 mg (Líquidos) | ||
PARÁGRAFO 1o. El término “Reducido” no puede utilizarse si el alimento de referencia cumple con los requisitos como “Bajo” aporte.
PARÁGRAFO 2o. El término “Reducido” debe aparecer en la etiqueta seguido inmediatamente de la preposición “en” y del nutriente o calorías que han sido objeto de reducción. Por ejemplo “Reducido en calorías”; “Reducido en grasa”.
PARÁGRAFO 3o. Los alimentos que cumplan con este descriptor, también podrán utilizar los siguientes sinónimos:” menos” o “más bajo en”, “ligero”, “liviano”, “menor”, “menor que”.
PARÁGRAFO 4o. El término light únicamente puede usarse para reducido en calorías.
21.2 Aumentado/más/más que/doble: la comparación deberá basarse en una diferencia relativa de al menos 25 % en el contenido de nutrientes respectivamente entre los alimentos comparados por porción.
ARTÍCULO 22. TÉRMINOS O DESCRIPTORES PERMITIDOS PARA LAS DECLARACIONES TIPO NO ADICIÓN. Se refiere a las características para utilizar la declaración de propiedades nutricionales del tipo “no adición” cuando a los alimentos no se les ha adicionado azúcares o sal/sodio, tal como se indica a continuación:
22.1 “Sin azúcares añadidos”, “sin azúcares agregados”, “sin azúcares adicionados”: se permite el descriptor si cumple las siguientes características:
a) No se ha añadido ningún tipo de azúcares a los alimentos, incluyendo, pero no limitándose a: sacarosa, glucosa, miel, melaza, jarabes o siropes, maltodextrinas, panela, melaza, néctar de agave, jugo de caña, dextrosa, azúcar turbinado, melaza negra, cristales de jugo de caña, zumo de caña evaporado, concentrado de fruta, zumo de fruta concentrado, sólidos de jarabe de maíz, maltosa, D- ribosa, sucrosa, sólidos de glucosa, cebada de malta, azúcar morena, caramelo, fructosa cristalina.
b) El alimento no contiene ningún ingrediente que contenga azúcares como ingrediente, incluyendo, pero no limitándose a: mermeladas, jaleas, chocolate con edulcorantes calóricos, trozos de frutas con edulcorantes calóricos, cereales azucarados, concentrados no reconstituidos de zumos de fruta.
c) No se utiliza algún medio, tal como el uso de enzimas, durante el procesado, que pueda incrementar el contenido de azúcares en el producto final (ejemplo: utilizando enzimas para hidrolizar almidones y liberar azúcares).
22.2 “Sin sal/sodio añadido”: se permite el descriptor si cumple las siguientes características:
a) El alimento no debe contener sal, ni otras sales o aditivos que contengan sodio.
b) El alimento no contiene ingredientes que contengan sal/sodio, incluyendo, pero no limitándose a: salsas, caldos deshidratados, alimentos en conserva, embutidos, sucedáneos de la sal, algas marinas, carnes marinadas, entre otros.
c) Debe cumplir con el requisito de “bajo en sodio”.
DECLARACIONES DE PROPIEDADES DE SALUD.
ARTÍCULO 23. REQUISITOS. Todo alimento que sea objeto de declaraciones de propiedades de salud, debe cumplir con los requisitos exigidos para la declaración de nutrientes y declaración de propiedades nutricionales del presente reglamento. El uso de declaraciones de propiedades de salud debe cumplir lo siguiente:
1. Deben basarse en una evidencia científica y el nivel de la prueba debe ser suficiente para establecer el tipo de efecto que se declara y su relación con la salud, como reconocido por datos científicos generalmente aceptables y la evidencia se debe revisar a la luz de nuevos datos.
2. Deben efectuarse de forma tal que, permita al público entender la información proporcionada y el significado de esa información con relación a una alimentación diaria.
3. La cantidad del alimento que debe consumirse para obtener el beneficio argumentado debe ser razonable en el contexto de una alimentación diaria.
4. Si existen otros factores determinantes para cumplir con los efectos sobre la salud se deben enunciar. Ejemplo: “Ejercicio físico regular y consumo de calcio”.
5. Si existen otros factores asociados a la enfermedad o trastorno de la salud se debe mencionar que esta depende de otros factores asociados. Ejemplo: “La enfermedad cardiovascular depende de muchos factores. Dietas bajas en grasa y colesterol pueden ayudar a disminuir el riesgo de enfermedad cardiovascular”.
6. Si el beneficio argumentado se atribuye a un nutriente en el alimento, para el cual se ha establecido un valor de referencia, dicho alimento debe ser: a) “Excelente en”, “buena fuente de” el nutriente, en el caso que se recomiende un incremento en el consumo; o, b) “Bajo en”, “reducido en”, o “libre del” nutriente, en el caso que se recomiende una reducción en el consumo.
7. Si el efecto anunciado en las declaraciones de propiedades de salud se atribuye a un nutriente o constituyente del alimento, deben estar disponibles los métodos analíticos validados y reconocidos internacionalmente para cuantificar el nutriente o constituyente declarado.
8. El alimento que declare propiedades de salud debe cumplir con los niveles que logran el efecto enunciado o asociado a la salud, establecidos de acuerdo con la evidencia científica.
9. La expresión de las declaraciones de propiedades de salud debe hacerse en términos condicionales, utilizando palabras como: “puede”; “podría”; “ayuda”; “contribuye a”.
10. La información relacionada con las declaraciones de propiedades de salud que se incluya en la etiqueta del producto, debe ser completa, verdadera, no confusa, ni engañosa, de conformidad con lo establecido en el presente reglamento.
PARÁGRAFO. Las declaraciones de propiedades de salud que ya habían sido aprobadas por la Sala Especializada de Alimentos y Bebidas del Invima, seguirán siendo vigentes, para el presente reglamento técnico.
ARTÍCULO 24. TIPOS DE DECLARACIONES DE SALUD. Las declaraciones son de tres tipos: 1. Declaración en función de nutrientes, 2. Otras declaraciones de propiedades de función y 3. Declaraciones de propiedades de reducción de riesgos de enfermedad:
24.1 Declaración de función de los nutrientes: describe la función fisiológica del nutriente en el crecimiento, el desarrollo y las funciones normales del organismo.
Ejemplo:
“El nutriente A (nombrando un papel fisiológico del nutriente A en el organismo respecto al mantenimiento de la salud y la promoción del crecimiento y del desarrollo normal). El alimento X es una fuente del/excelente en el nutriente A”, dentro de una alimentación completa.
24.2 Otras declaraciones de propiedades de función: Estas declaraciones de propiedades conciernen efectos benéficos específicos del consumo regular de alimentos o sus constituyentes en el contexto de una dieta total sobre las funciones o actividades biológicas normales del organismo. Tales declaraciones de propiedades se relacionan a una contribución positiva a la salud o a la mejora de una función o la modificación o preservación de la salud.
Ejemplo:
“La sustancia A (nombrando los efectos de la sustancia A sobre el mejoramiento o modificación de una función fisiológica o la actividad biológica asociada con la salud). El alimento Y contiene X gramos de sustancia A”.
Para efectos del presente reglamento técnico, se señalan algunas declaraciones de propiedades de otras funciones y sus características generales:
24.2.1. Declaraciones que relacionan el consumo de probióticos con una mejor función digestiva:
a) El microorganismo o bacteria debe cumplir lo siguiente:
- Estar vivo, no ser patógeno y su medio natural es el tracto digestivo humano.
- Ser capaz de sobrevivir en el tracto intestinal, es decir, ser resistente a los jugos gástricos y los ácidos biliares.
- Tener la capacidad de adherirse a la mucosa intestinal.
- Tener la capacidad de colonizar el intestino.
- Tener la capacidad de sobrevivir a lo largo de la vida útil del producto al cual se adiciona.
b) El alimento debe contener un número mayor o igual de bacterias viables de origen probiótico a 1 x 106 UFC/g en el producto terminado hasta el final de la vida útil.
c) La declaración debe indicar que el consumo adecuado y regular de microorganismos probióticos no es el único factor para mejorar las funciones digestivas y que existen otros factores adicionales a considerar como el ejercicio físico y el tipo de dieta.
d) Modelo de declaración: “Una adecuada alimentación y un consumo regular de alimentos con microorganismos probióticos, puede ayudar a normalizar las funciones digestivas y regenerar la flora intestinal”.
24.2.2. Declaraciones de propiedades de salud que relacionan el consumo de prebióticos con una mejor función intestinal:
a) La sustancia considerada como prebiótico debe cumplir lo siguiente:
- La cantidad de alimento que debe consumirse, para obtener el efecto benéfico debe ser razonable en el contexto de la dieta diaria.
- Ser una sustancia preferida por una o más especies de bacterias benéficas en el intestino grueso o colon.
- Ser resistente a los ácidos gástricos (a la acidez gástrica).
- Ser fermentables por la microflora intestinal.
- Ser resistente a la hidrólisis enzimática endógena.
- Tener la capacidad de producir cambios en el lumen del intestino grueso o en el organismo del huésped que muestra beneficios para la salud.
- Estimular selectivamente el crecimiento y/o la actividad de aquellas bacterias que están asociadas con la salud y el bienestar.
b) La declaración debe indicar que el consumo adecuado y regular con prebióticos no es el único factor para mejorar las funciones digestivas y que existen otros factores adicionales a considerar tales como el ejercicio físico y el tipo de alimentación.
c) Modelo de declaración: “Una dieta adecuada y el consumo regular de mínimo X g al día de prebióticos Y, promueve una flora intestinal saludable/buena/balanceada”; “Beneficia la flora intestinal”; “Ayuda en el mejoramiento intestinal /función digestiva”.
24.3 Declaraciones de propiedades de reducción de riesgos de enfermedad: La declaración consiste en dos partes: (i) información sobre el papel fisiológico del nutriente sobre una relación conocida entre la salud y la dieta; seguida por (ii) información sobre la composición del producto pertinente al papel fisiológico del nutriente en esta relación, a no ser que la relación esté basada en un alimento completo o alimentos que las investigaciones no vinculen con constituyentes específicos del alimento.
PARÁGRAFO 1o. El beneficio alegado debería proceder del consumo regular de una porción de un alimento, (definida en el artículo 12 del presente documento), o constituyente alimentario en el contexto de una dieta saludable. Si el beneficio alegado se atribuye a un constituyente en el alimento para el cual se ha establecido un Valor de Referencia de Nutrientes (VRN), el alimento en cuestión debería ser:
(i) una fuente excelente del constituyente en el caso en que se recomiende un incremento en el consumo; o, (ii) bajo en, reducido en, o libre del constituyente en el caso en que se recomiende una reducción en el consumo.
PARÁGRAFO 2o. Cuando sea aplicable, las condiciones para las declaraciones de propiedades nutricionales y comparativas se utilizarán para establecer los niveles para “excelente fuente”, “bajo en”, “reducido en”, o “libre de”, acompañado de: “en una dieta saludable puede reducir el riesgo”.
ARTÍCULO 25. PROHIBICIONES EN DECLARACIONES EN SALUD. <Artículo modificado por el artículo 4 de la Resolución 2492 de 2022. El nuevo texto es el siguiente:> Están prohibidas las siguientes declaraciones:
25.1. Las declaraciones de propiedades en salud no deben sugerir que el alimento por sí solo es suficiente para la alimentación diaria ni tampoco que la alimentación equilibrada con base en alimentos comunes no suministra las cantidades suficientes de todos los elementos nutritivos.
25.2. Las declaraciones de propiedades en salud no deben promover el consumo excesivo de cualquier alimento, ni ser contrarias a los buenos hábitos alimentarios establecidos en las Guías Alimentarias Basadas en Alimentos para la población colombiana.
25.3. Las declaraciones de propiedades en salud no deben generar dudas sobre la inocuidad y calidad de alimentos similares.
25.4. Cuando un producto cuente con 1 o más sellos frontales de advertencia, no podrá realizar declaraciones de propiedades de salud.
25.5. No se permite cuantificar el grado de reducción del riesgo de enfermedad causados por los factores metabólicos atribuibles a las ENT.
25.6. Las declaraciones de propiedades de salud no deben implicar en ningún caso propiedades curativas, medicinales ni terapéuticas.
25.7. El término “saludable” o cualquier término derivado de este, como: “salud”, “salubre”, “saludablemente”, “salubridad”, “buena salud”, “estado sano”, no puede ser usado en el rotulado o etiquetado de un alimento para describirlo como “saludable” ni presentarlo, de modo que se pueda suponer que el alimento en sí comunica “salud”.
25.8. Los términos “alimento completo”, “nutrición balanceada”, “nutrición completa” o equivalentes, con los cuales se pueda suponer que un alimento por sí so/o es suficiente para la alimentación diaria, no podrán ser usados.
ARTÍCULO 26. AUTORIZACIÓN PARA OTRAS DECLARACIONES DE PROPIEDADES DE SALUD. Previa comercialización del producto, se aceptarán las declaraciones de propiedades que ya hayan cumplido con los criterios de declaraciones de propiedades de salud de función de nutrientes establecidos en el acta de la SEAB número 4 y 13 del 2017, de no cumplir con los criterios allí mencionados deberá acogerse al protocolo de aprobación definido en la Resolución número 684 de 2012.
ESPECIFICACIONES Y FORMATOS DE LA TABLA DE INFORMACIÓN NUTRICIONAL Y DEL ETIQUETADO FRONTAL.
ARTÍCULO 27. ESPECIFICACIONES DE LA TABLA DE INFORMACIÓN NUTRICIONAL. La tabla de información nutricional cumplirá las condiciones generales y específicas que se establecen a continuación:
27.1 Condiciones generales.
27.1.1 La información nutricional deberá aparecer agrupada, presentada en un recuadro, en un lugar visible de la etiqueta, con tamaño mínimo del 25% del área disponible para impresión de la cara en donde se ubique (preferiblemente cara posterior), en caracteres legibles y en color contrastante con el fondo donde esté impresa.
27.1.2 La información nutricional deberá incluir las cifras y las unidades correspondientes a cada nutriente declarado.
27.1.3 La información nutricional debe aparecer en idioma español y adicionalmente podrá figurar en otro idioma. En caso de que en la etiqueta original aparezca la información en otro idioma o en español, se debe utilizar un rótulo o etiqueta complementaria y adherida en lugar visible, con la traducción y requisitos del presente reglamento técnico.
Este rótulo complementario se puede utilizar en productos importados con etiqueta original en español que requieran expresar la información nutricional, de acuerdo con los requisitos establecidos en el presente reglamento, y su ajuste se podrá realizar antes, durante o después del proceso de nacionalización, el cual puede ir en cualquier parte del producto.
27.1.4 El tipo de letra de la información nutricional debe ser Arial o Helvética, de fácil lectura.
27.1.5 La información sobre energía, nutrientes puede declararse utilizando las abreviaturas permitidas de conformidad con lo establecido en el Capítulo II del presente reglamento.
27.1.6 Para el caso de los productos importados se permite el uso de los formatos de tablas nutricionales de otro país, no obstante, debe incluirse la tabla nutricional para Colombia cumpliendo con todos los requisitos establecidos en el presente reglamento técnico, si el producto y/o materia prima tiene alcance normativo en la presente resolución.
ARTÍCULO 28. CONDICIONES ESPECÍFICAS.
28.1 El título de la Tabla de Información Nutricional debe declararse como “Información Nutricional” o “Datos de Nutrición” o “Información Nutrimental” utilizando el tipo letra Arial o Helvética, en un tamaño mínimo de 10 puntos. Los títulos y los nombres de los siguientes datos nutricionales: calorías, grasa saturada, grasas trans, azúcares añadidos y sodio, deben aparecer en negrilla y tener un tamaño de letra 1.3 veces más grande para distinguirlos de los demás nutrientes.
28.2 El nombre de cada nutriente, debe aparecer en una columna seguido inmediatamente por la cantidad en peso del nutriente, usando “g” para gramos o “mg” para miligramos, “íg” microgramos o UI (unidades internacionales), según corresponda.
28.2.1 La declaración de grasa saturada, monoinsaturada, poliinsaturada (cuando corresponda de ácidos omega-3) y grasa trans debe aparecer en este orden en forma de sangría inmediatamente debajo de la declaración de grasa total.
28.2.2 La declaración de fibra dietaria y cuando aplique de polialcoholes, a su vez, la declaración de azúcares añadidos (cuando aplique) con sangría inmediatamente debajo de los azúcares totales y azúcares totales debe aparecer en forma de sangría inmediatamente debajo de la declaración de carbohidratos totales y, cuando corresponda, la declaración de fibra soluble e insoluble debe aparecer en este orden en forma de sangría inmediatamente debajo de la declaración de fibra dietaria.
28.3 La información sobre vitaminas y minerales, excepto sodio y potasio, debe separarse de la información de los demás nutrientes con una línea y presentarse verticalmente en una o dos líneas, utilizando el tipo de letra Arial o Helvética, en un tamaño mínimo de 5 puntos. Si se declara potasio, su información debe aparecer inmediatamente debajo de la de sodio.
28.4 Los datos nutricionales deben aparecer en el siguiente orden: calorías, grasa total, grasa saturada, grasa trans, carbohidratos, fibra dietaria, azúcares totales, azúcares añadidos, proteína, y sodio. Los nombres y sus datos nutricionales de los siguientes nutrientes: calorías, sodio, grasa saturada, grasas trans y azúcares añadidos, deben estar en negrilla y tener la letra 1.3 veces más grande en tamaño que las demás. En el caso de que solo sean declaradas las Vitaminas y minerales de obligatoria declaración, el orden será: Vitamina A, Vitamina D, Hierro, Calcio y Zinc, de lo contrario, si se declaran más vitaminas y minerales, entonces seguirán el orden de aparición como el de la Tabla 9.
28.5 Para los campos de tamaño de porción y número de porciones por envase se utilizará el tipo de letra Arial o Helvética en un tamaño mínimo de 10 puntos.
ARTÍCULO 29. FORMATOS DE TABLA DE INFORMACIÓN NUTRICIONAL. La tabla de Información Nutricional debe presentarse en uno de los siguientes tipos de formato, dependiendo del área de impresión disponible en la etiqueta, nutrientes declarados, formas y otras consideraciones del alimento:
a) Vertical estándar;
b) Simplificado;
c) Tabular y lineal.
ARTÍCULO 30. ESPECIFICACIONES DE LOS FORMATOS DE TABLA DE INFORMACIÓN NUTRICIONAL. Las siguientes son las especificaciones que deben cumplir cada uno de los formatos para tabla de información nutricional:
PARÁGRAFO. En el caso de los alimentos envasados que se consuman reconstituidos, acorde a las condiciones de consumo definidas por el fabricante, la tabla de información nutricional se presentará como sólido (por 100 g) o líquido (por 100 mL) y por porción lista para consumir. Los títulos de las columnas se indicarán en su orden: por 100 g o por 100 mL y por porción preparada.
30.1 Formato vertical estándar. El formato vertical estándar debe presentar la información indicada en el artículo 10 del presente reglamento en forma de columna, tal como se muestra en el ejemplo de la Figura 1. El grosor de las líneas del recuadro de las líneas de separación de los segmentos y nutrientes, definidas para este formato, puede variar; y se aplicará igualmente cuando se utilicen los formatos tabular, lineal y simplificado.
Figura 1. Formato vertical estándar
| Información Nutricional | ||
| Tamaño de porción: 1 unidad (40 g) | ||
| Número de porciones por envase: Aprox. 2 | ||
| Calorías (kcal) | Por 100 g | Por porción |
| 261 | 101 | |
| Grasa total | 13 g | 5.2 g |
| Grasa poliinsaturada | 3.0 g | 1.2 g |
| Grasa saturada | 6.0 g | 2.4 g |
| Grasa trans | 820 mg | 328 mg |
| Carbohidratos totales | 31 g | 12 g |
| Fibra dietaria | 0.8 g | 0.3 g |
| Azúcares totales | 5.0 g | 2.0 g |
| Azúcares añadidos | 2.0 g | 0.8 g |
| Proteína | 5.0 g | 2.0 g |
| Sodio | 560 mg | 224 mg |
| Vitamina A | 3.0 íg ER | 1.2 íg ER |
| Calcio | 400 mg | 160 mg |
| Hierro | 4.0 mg | 1.6 mg |
| Vitamina D | 5.0 íg | 2.0 íg |
| Vitamina B1 | 1.01 mg | 0.41 mg |
| Zinc | 4.0 mg | 1.6 mg |
PARÁGRAFO. Para el caso de carne cruda a la que se le han agregado productos alimenticios, condimentos o aditivos que contengan sodio, la declaración de contenido de sodio, deberá realizarse de la siguiente manera:
Figura 2. Formato para carnes crudas con adición de productos alimenticios, condimentos o aditivos que contengan sodio
| Información Nutricional | ||
| Tamaño de porción: 1 unidad (40 g) | ||
| Número de porciones por envase: Aprox. 2 | ||
| Sodio (mg) | Por 100 g | Por porción |
| 560 | 224 | |
30.2 Formato simplificado. El formato simplificado, puede ser usado cuando un alimento contiene cantidades no significativas o no es fuente significativa de seis (6) o más de los siguientes datos nutricionales: calorías/kilocalorías, grasa total, grasa saturada, grasa trans, sodio, carbohidratos totales, fibra dietaria, azúcares totales, azúcares añadidos, proteína, vitamina A, vitamina D, hierro, calcio y zinc. Para este efecto “cantidad no significativa” o “no es fuente significativa”, se establece en el Capítulo II de este reglamento.
El formato simplificado debe tener la misma presentación gráfica en forma de columna del formato vertical estándar, como se muestra en la figura 3, e incluir:
a) La siguiente información:
- Calorías totales, grasa total, grasa saturada, grasa trans, carbohidratos totales, proteína, sodio, azúcares totales y azúcares añadidos.
- Cualquier otro nutriente de declaración obligatoria si están presente en cantidades mayores a las no significativas.
c) La frase “No es fuente significativa de (…)”. Indicando en el espacio de los puntos suspensivos aquellos nutrientes identificados como cantidades no significativas) en la parte inferior de la tabla de Información Nutricional;
Figura 3. Formato simplificado
| Información Nutricional | ||
| Tamaño de porción: 1 unidad (40g) Número de porciones por envase: Aprox. 2 | ||
| Calorías (kcal) | Por 100g | Por porción |
| 241 | 96 | |
| Grasa total | 13 g | 5.2 g |
| Grasa saturada | 6.0 g | 2.4 g |
| Grasa trans | 820 mg | 328 mg |
| Carbohidratos totales | 31 g | 12 g |
| Azúcares totales | 5.0 g | 2.0 g |
| Azúcares añadidos | 2.0 g | 0.8 g |
| Sodio | 560 mg | 224 mg |
| No es fuente significativa de Proteína, Vitamina D, Hierro, Calcio, Zinc, Vitamina A y fibra. | ||
30.3 Formatos tabular y lineal. Los formatos tabular o lineal se pueden usar en el caso de envases cuya área disponible de impresión en la etiqueta del producto es menor a 225 cm2.
30.4 Formato tabular. El Formato Tabular debe presentar la información nutricional en forma horizontal dispuesta en cuatro columnas, como se muestra en la Figura 4.
Figura 4. Formato tabular
| Información Nutricional | Calorías | Por 100 g | Por porción |
| 261 kcal | 101 kcal | ||
| Grasa total | 13 g | 5.2 g | |
| Grasa saturada | 6.0 g | 2.4 g | |
| Grasa Trans | 820 mg | 328 mg | |
| Tamaño de porción: 1 | Sodio | 560 mg | 224 mg |
| unidad (40 g) Número | Carbohidratos totales | 31 g | 12 g |
| de porciones por | Fibra dietaria | 0 g | 0 g |
| envase: Aprox. 2 | Azúcares totales | 5.0 g | 2.0 g |
| Azúcares añadidos | 2.0 g | 0.8 g | |
| Proteína | 5.0 g | 2.0 g | |
| Calcio | 400 mg | 160 mg | |
| No es fuente significativa de Vitamina A, Vitamina D, Hierro, Calcio y Zinc. | |||
30.5 Formato lineal
Información nutricional (100 g o 100 mL): Calorías 261, Grasa total 13.0 g, Sodio 560 mg, Carbohidratos totales 31 g, Azúcares añadidos 2.0 g, Proteína 5.0 g, Vitamina A 4.0 íg ER, Vitamina D 5.0 íg, Hierro 4.0 mg y Zinc 3.0 mg.
Información nutricional (porción): Tamaño de porción: 1 unidad (40 g) Número de porciones por envase: Aprox. 2 porciones Calorías 101, Grasa total 5.2 g, Sodio 224 mg, Carbohidratos totales 12.0 g, Azúcares añadidos 0.8 g, Proteína 2.0 g, Vitamina A 1.2 íg ER, Vitamina D 2 íg, Hierro 1.6 mg y Zinc 1.6 mg. No es fuente significativa de grasa saturada, grasa trans, calcio y fibra
El formato lineal se puede utilizar solamente cuando no es posible por tamaño y forma, incluir en la etiqueta el formato tabular. Se listarán los nutrientes por 100 g - mL y por porción. Deben estar en negrilla las calorías y los siguientes nutrientes: grasa saturada, grasas trans, sodio y azúcares añadidos.
Los nutrientes deben estar seguidos, separados por comas.
Figura 5. Formato Lineal
ARTÍCULO 31. TABLA DE INFORMACIÓN NUTRICIONAL PARA PRODUCTOS EN EMPAQUES SECUNDARIOS, PAQUETES MÚLTIPLES, SURTIDOS O MIXTOS. Deben cumplir las siguientes especificaciones:
31.1 Productos en empaque secundario:
a) Para alimentos que se comercializan en empaques primarios individuales contenidos en un mismo empaque secundario, destinados para la venta al público, la tabla de información nutricional, el etiquetado de advertencia y el sello positivo, si aplica; de cada alimento debe aparecer sobre el envase exterior ofrecido al público. El tamaño máximo de cada una de esas tablas debe ser el mismo que el de la tabla que se pondría en cada uno de los empaques primarios, en proporción con la cantidad de productos en el empaque secundario.
b) Para aquellos alimentos cuyo empaque individual es en envases de materiales de origen natural, el empaque secundario será el que presente la tabla de información nutricional, el etiquetado de advertencia y el sello positivo, si aplica;
31.2 Productos en paquetes múltiples. Para productos que consisten en dos o más alimentos empacados individualmente, contenido en un envase exterior y destinado para su consumo por separado, la información nutricional, el etiquetado frontal de advertencia y el sello positivo, si aplica, debe ser especificada para cada alimento en un lugar claramente visible al consumidor. Adicionalmente el empaque secundario deberá tener la tabla nutricional de cada una de las referencias de producto contenidas en dicho empaque. En este último caso, el tamaño máximo de dicha tabla debe ser el mismo que el de la tabla que se pondría en cada uno de los empaques primarios en proporción con la cantidad de productos en el empaque secundario
31.3 Productos en empaques surtidos o mixtos: deben cumplir las siguientes características:
a) Para productos alimenticios consistentes en dos o más paquetes individuales de ingredientes, ambos contenidos en otro envase exterior, destinados para la venta al público, la tabla de información nutricional, el etiquetado de advertencia y el sello positivo, si aplica, debe aparecer sobre el envase exterior ofrecido al público, identificando de manera clara la información por cada uno de los ingredientes;
b) Cuando los productos surtidos son empacados en forma individual, con la intención de que el consumidor los ingiera al mismo tiempo, la información nutricional, el etiquetado de advertencia y el sello positivo, si aplica, debe ser especificada para cada producto o para su mezcla.
31.4 Envases pequeños y pirograbados
Los alimentos en envases pequeños, con una superficie total para etiquetado menor a 77 cm2, deben incluir la tabla de información nutricional, el etiquetado de advertencia y el sello positivo, si aplica en el envase secundario, cuando lo contenga. Estos envases deben incluir una dirección electrónica o número de teléfono, o cualquier otro medio, que el consumidor pueda utilizar para obtener la información nutricional. Para aplicación de esta excepción se entenderá por superficie total la suma de las áreas de todas las superficies impresas del material de empaque excluyendo las áreas de sellado.
31.5 Envases retornables: Los productos en envases de vidrio retornables cuya superficie total para etiquetado sea mayor a 77 cm2 deben incluir: un código QR, una dirección electrónica o número telefónico, en el cual el consumidor pueda ver la tabla de información nutricional, el etiquetado de advertencia y el sello positivo, si aplica, y/o declaraciones nutricionales del producto.
ARTÍCULO 32. ETIQUETADO FRONTAL DE ADVERTENCIA. <Artículo corregido por el artículo 1 de la Resolución 254 de 2023. El nuevo texto es el siguiente:> Cuando a un producto alimenticio procesado o ultraprocesado envasado se le haya adicionado sal/sodio, azúcares, grasas o edulcorantes y su contenido sea igual o superior al valor establecido en la Tabla número 17, deberá rotular la o las características nutricionales relativas al nutriente adicionado.
Tabla número 17 Límites de contenidos de nutrientes para establecimiento de sello de advertencia
| Nutriente | Sólidos (100 g) - semisólidos | Líquidos (100 mL) |
| Sodio | >= 1mg/kcal y/o >= 300 mg/100 g Para carnes crudas envasadas a las que se les haya adicionado sal/sodio, el límite es 300 mg/100 g | >= 1mg/kcal o Bebidas analcohólicas sin aporte energético: = 40 mg de sodio cada 100 ml |
| Azúcares | >= 10% del total de energía proveniente de azúcares libres | >= 10% del total de energía proveniente de azúcares libres |
| Grasas saturadas | >= 10% del total de energía proveniente de grasas saturadas | >= 10% del total de energía proveniente de grasas saturadas |
| Grasas trans | >= 1% del total de energía proveniente de grasas trans | >= 1% del total de energía proveniente de grasas trans |
| Edulcorantes | Cualquier cantidad de edulcorantes | Cualquier cantidad de edulcorantes |
32.1. Para la aplicación de la tabla anterior deberán tenerse en cuenta las siguientes reglas:
a) Para efectos de este artículo, se entenderá que un alimento es sólido o líquido según la unidad de medida utilizada en la declaración del contenido neto del alimento, es decir, será sólido si su contenido neto está expresado en unidades de masa según el sistema internacional de unidades, o líquido si su contenido neto está expresado en unidades de volumen según el sistema internacional de unidades. Los alimentos envasados que se consuman reconstituidos se entenderán como sólidos o líquidos, según como sea el producto listo para consumir, de acuerdo con las instrucciones de reconstitución definidas por el fabricante. Estas instrucciones pueden incluir la cocción.
b) Se entenderá por producto alimenticio procesado o ultraprocesado envasado que se les haya adicionado sal/sodio a aquellos a los que durante el proceso de elaboración se haya utilizado como ingrediente o aditivo cualquier sal o aditivo que contenga sodio o cualquier ingrediente que contenga sales de sodio agregadas.
c) Se entenderá por producto alimenticio procesado o ultraprocesado envasado que se les haya adicionado azúcares aquellos que cumplan con la definición de azúcares libres, definidos en la Resolución 3803 de 2016, o en la que la modifique o sustituya.
d) Se entenderá por producto alimenticio procesado o ultraprocesado envasado que se les haya adicionado grasas aquellos a los que durante el proceso de elaboración se haya utilizado como ingrediente grasas vegetales o animales, aceites vegetales parcialmente hidrogenados (manteca vegetal, crema vegetal o margarina) e ingredientes que los contengan agregados.
e) Se entenderá por producto alimenticio procesado o ultraprocesado envasado que se les haya adicionado edulcorantes, aquellos a los que durante el proceso de elaboración se haya utilizado como ingrediente o aditivo, edulcorantes o ingredientes que los contengan agregados.
32.2. <Numeral será modificado a partir del 23 de abril de 2026 por el artículo 6 de la Resolución 2066 de 2024. El texto HASTA ESTA FECHA es el siguiente:> Para calcular los porcentajes establecidos en la tabla 17, se procederá, de la siguiente manera:
a) Sodio: para el caso de sodio, debe realizar dos cálculos, si alguno de los dos, resulta igual o superior a la cantidad establecida, debe etiquetar el sello de advertencia de sodio: 1. Primer cálculo: si es un alimento sólido o bebida con calorías, se toma cualquier cantidad de alimento, puede ser 100 g o ml, o la porción, y se divide el contenido de sodio declarado, entre el número de kcal, declaradas en la misma cantidad, si esta relación es igual o superior a 1, debe etiquetar el sello de advertencia de sodio. 2. Segundo cálculo: Debe calcular el contenido de sodio en 100 g o ml y si este es igual o supera los 300 mg, debe etiquetar el sello de advertencia de sodio. Ahora bien, para las bebidas sin aporte energético o sin calorías, se debe calcular el contenido en 100 ml, y si este supera o es igual a 40 mg, debe etiquetar el sello frontal de advertencia de sodio.
b) Azúcares: se debe identificar los azúcares libres del alimento, según lo establecido en la Resolución 3803 de 2016 o en la que modifique o sustituya. Una vez identificados, en cualquier cantidad de alimento, se debe multiplicar la cantidad de azúcares libres en gramos, por el factor de conversión de azúcares (4 kcal / g). Este resultado se divide entre el total de las kcal, de la misma cantidad de alimento y se multiplica por 100. Finalmente, se compara este resultado con el porcentaje establecido en la tabla 17, y si es igual o superior a 10%, debe etiquetar el sello de advertencia de azúcares. Adicionalmente, para contabilizar los azúcares libres a partir de los azúcares añadidos, se debe partir de los azúcares añadidos y adicionarles los azúcares presentes en jugos de frutas y/o verduras.
c) Grasas saturadas: se debe multiplicar la cantidad de grasas saturadas en gramos, por el factor de conversión de grasas (9 kcal / g), en cualquier cantidad de alimento. Este resultado se divide entre el total de las kcal, de la misma cantidad de alimento y se multiplica por 100. Finalmente, se compara este resultado con el porcentaje establecido en la tabla 17, y si es igual o superior a 10%, debe etiquetar el sello frontal de advertencia de grasas saturadas.
d) Grasas trans: se debe multiplicar la cantidad de grasas trans en gramos, por el factor de conversión de grasas (9 kcal / g), en cualquier cantidad de alimento. Este resultado se divide entre el total de las kcal, de la misma cantidad de alimento y se multiplica por 100. Finalmente, se compara este resultado con el porcentaje establecido en la tabla 17, y si es igual o superior a 1%, debe etiquetar el sello frontal de advertencia de grasas trans.
32.3. Forma del sello frontal de advertencia: la forma de destacar las características nutricionales indicadas en el inciso primero de este artículo será incluyendo sellos en la etiqueta, los cuales consistirán en un símbolo octagonal de fondo color negro y borde blanco, y en su interior el texto “EXCESO EN”, seguido de: “GRASAS SATURADAS” o “GRASAS TRANS” o “SODIO” o “AZÚCARES” o con el texto “CONTIENE EDULCORANTES” de manera individual o con 2 o 3 o 4 o 5 sellos (según corresponda). Las letras del texto de los sellos deberán ser mayúsculas y de color blanco, tipo de letra ARIAL BOLD. Además, en el mismo símbolo, deberá inscribirse en letras blancas, la palabra “MINSALUD”, según la figura 6 del presente artículo.
FIGURA 6. Forma del sello frontal de advertencia

No se puede utilizar otro formato de etiquetado frontal, ni tipo de forma de sello de advertencia, ni cambiar el texto, tipo de letra, diagrama o dibujo, en ningún producto, independiente si lleva o no, etiquetado frontal de advertencia. No se puede utilizar la forma del etiquetado frontal de advertencia para incluir sellos con un texto diferente que haga alusión a otros nutrientes o cualquier componente de los productos envasados diferente a los que son objeto de esta regulación (sal/sodio, azúcares, grasas, edulcorantes).
32.4. Dimensiones y ubicación del sello de advertencia: el o los símbolos referidos se ubicarán en el tercio superior derecho de la cara frontal (o cara principal de exhibición) de la etiqueta de los productos. Para el caso de los envases cilíndricos y cónicos, los sellos deberán colocarse en el tercio superior central. Las dimensiones del o los símbolos referidos estarán determinadas de acuerdo con el área de la cara principal de exhibición de la etiqueta, según la siguiente tabla:
Tabla 18. Dimensiones del sello de advertencia
| Área de la cara principal de la etiqueta (cm2) | Sello ancho y alto (en cm) |
| <30 cm2 | Rotula en envase secundario y si no cuenta con él, se debe incluir un código QR o una página de internet donde se pueda consultar |
| >= 30 cm2 a < 35 cm2 | 1.7 x 1.7 cm |
| >= 35 cm2 a < 40 cm2 | 1.8 x 1.8 cm |
| >= 40 cm2 a < 50 cm2 | 2.0 x 2.0 cm |
| >= 50 cm2 a < 60 cm2 | 2.2 x 2.2 cm |
| >= 60 cm2 a < 80 cm2 | 2.5 x 2.5 cm |
| >= 80 cm2 a < 100 cm2 | 2.8 x 2.8 cm |
| >= 100 cm2 a < 125 cm2 | 3.1 x 3.1 cm |
| >= 125 cm2 a < 150 cm2 | 3.4 x 3.4 cm |
| >= 150 cm2 a < 200 cm2 | 3.9 x 3.9 cm |
| >= 200 cm2 a < 250 cm2 | 4.4 x 4.4 cm |
| >= 250 cm2 a <= 300 cm2 | 4.8 x 4.8 cm |
| > 300 cm2 | 15% del tamaño de la cara principal |
32.4.1. Cuando corresponda rotular más de un símbolo con el descriptor “EXCESO EN”, estos deberán estar dispuestos uno junto con el otro o uno debajo del otro, teniendo en cuenta las formas descritas en el numeral 32.3 del presente artículo.
32.4.2. Para los productos que deban llevar dos (2) o más sellos, se deberá determinar el área de la cara principal disponible para los sellos (ADS), así:
a) Para superficies con área de la cara principal de los envases mayor o igual a 30 cm2 y menor o igual a 300 cm2, el ADS debe considerarse el 65% del resultado obtenido de las especificaciones de “cálculo del área de la cara principal de los envases”.
b) Para superficies con área de la cara principal de los envases mayores a 300 cm2, según la tabla 18 le corresponde un único tamaño de sello octogonal de 3,9 cm x 3,9 cm.
32.4.3. El o los símbolos deberán rotularse de modo visible, indeleble y fácil de leer en circunstancias normales de compra y uso. En ningún caso podrán ser cubiertos total o parcialmente.
32.5. Proporciones del sello de advertencia: Todos los elementos (textos e íconos) deben estar centrados sobre el eje y del cuadro negro. A continuación, se presenten las proporciones. La letra “x” corresponde a la unidad de proporción sobre la que se construye el ícono del sello.
32.5.1. Sodio. La letra “x” corresponde a la unidad de proporción sobre la que se construye el ícono del sello.

32.5.2. Grasas saturadas. La letra “x” corresponde a la unidad de proporción sobre la que se construye el ícono del sello.

32.5.3. Grasas trans. La letra “x” corresponde a la unidad de proporción sobre la que se construye el ícono del sello.

32.5.4. Azúcares. La letra “x” corresponde a la unidad de proporción sobre la que se construye el ícono del sello.

32.5.5. Edulcorantes. La letra “x” corresponde a la unidad de proporción sobre la que se construye el ícono del sello.

32.5.6. Formas de distribución.
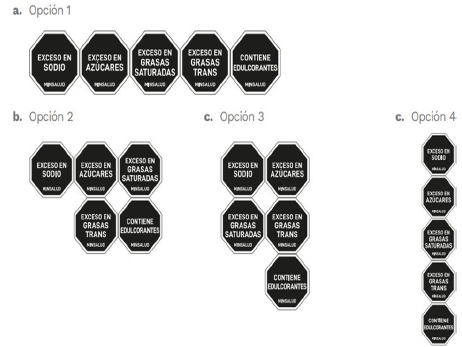
PARÁGRAFO. Se podrán también utilizar adhesivos en la etiqueta de modo indeleble, siempre que los mismos cumplan los requisitos de características, tamaño y ubicación definidos en este acto administrativo. El adhesivo deberá estar fijado de forma segura mediante adhesión, impresión, cosido, gofrado, serigrafía, termofijación, u otros medios análogos, de tal forma que se garantice que no se desprenda del producto en las condiciones normales de uso, conservación, almacenamiento, transporte y permanezca adherido hasta el momento de su comercialización y vida útil.
ARTÍCULO 33. SELLO POSITIVO. Cuando el alimento envasado cumpla con todos los siguientes criterios técnicos, puede de manera voluntaria incluir el sello positivo, cumpliendo con las características, tamaños y ubicación definidos en el presente reglamento técnico.
33.1 Cumplir con los siguientes contenidos máximos para sodio, grasa saturada y azúcares añadidos:
Tabla 19. Contenidos máximos para sodio, azúcares añadidos y grasas saturadas
| Nutriente | Sólidos (100 g) | Líquidos (100 mL) |
| Sodio (mg) | <=80 | <=60 |
| Azúcares añadidos (g) | <=2.0 | <=1.0 |
| Grasas saturadas (g) | <=2.0 | <=2.0 |
33.2 Su primer ingrediente en la lista de ingredientes no puede ser: sodio o aditivos con sodio, grasas y/o azúcares añadidos.
33.3 No se usen, en su formulación, edulcorantes calóricos y/o no calóricos.
33.4 Forma del sello positivo: La forma de destacar las características nutricionales indicadas en los numerales 33.1, 33.2 y 33.3, será etiquetando con un símbolo de visto bueno color RGB (34, 55, 98) o CMYK (100%, 87%, 33%, 22%) y un visto bueno de color blanco en su exterior, tal como se muestra en la siguiente figura:
Figura 7. Forma del sello positivo

PARÁGRAFO. No se puede utilizar otro tipo de forma de sello positivo, ni cambiar el color, añadir letras o frases, ni tamaños, ni ubicación.
33.5 Dimensiones y ubicación del sello de positivo: El símbolo referido se ubicará en la parte inferior izquierda de la cara frontal de la etiqueta de los productos. Las dimensiones del o los símbolos referidos estarán determinadas de acuerdo al área de la cara principal de exhibición de la etiqueta, según la siguiente tabla:
Tabla 20. Dimensiones del sello positivo
| Área de la cara principal de la etiqueta (cm2) | Dimensiones de símbolo (lado más largo) |
| < 30 | Rotula en el envase mayor que los contenga |
| >= 30 y <60 | 1.4 cm |
| >= 60 y <100 | 1.8 cm |
| >= 100 y <200 | 2.5 cm |
| >=200 y <300 | 3.0 cm |
| >= 300 | 3.5 cm |
Proporciones
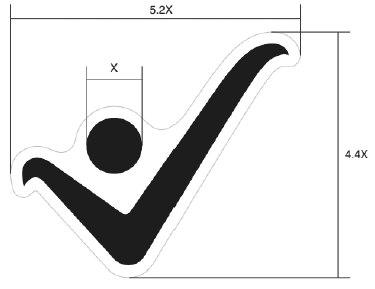
La letra “x” corresponde a la unidad de proporción sobre la que se construye el ícono del sello.
EVALUACIÓN DE LA CONFORMIDAD.
ARTÍCULO 34. PROCEDIMIENTO DE EVALUACIÓN DE LA CONFORMIDAD. Para efectos de evaluación de la conformidad del presente reglamento técnico, la información de las declaraciones de propiedades nutricionales, las declaraciones de propiedades de salud y el etiquetado frontal serán establecidas como declaración de primera parte manifestada por el productor, comercializador, o importador, o quien corresponda. Esta declaración presume que el declarante, ha efectuado por su cuenta, las verificaciones, inspecciones y los ensayos requeridos, y por tanto proporciona bajo su responsabilidad que los alimentos empacados o envasados cumplen con lo establecido en el presente reglamento técnico.
RESPONSABILIDAD, INSPECCIÓN, VIGILANCIA Y CONTROL.
ARTÍCULO 35. RESPONSABILIDAD. Las personas naturales o jurídicas que se dediquen al procesamiento, comercialización y/o importación de los alimentos envasados y empacados para el consumo humano serán responsables del cumplimiento de los requerimientos sanitarios contemplados en la reglamentación sanitaria y de lo dispuesto en el presente reglamento técnico.
ARTÍCULO 36. INSPECCIÓN, VIGILANCIA Y CONTROL. Corresponde al Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima) ejercer las funciones de inspección, vigilancia y control, en coordinación con las entidades territoriales del orden departamental o distrital, y en desarrollo del Modelo de Inspección, Vigilancia y Control Sanitario, definido por el Ministerio de Salud y Protección Social mediante Resolución número 1229 de 2013 o la norma que la modifique o sustituya, para lo cual podrán aplicar las medidas de seguridad e imponer las sanciones correspondientes, de conformidad con lo establecido en la Ley 9a de 1979 y el procedimiento administrativo sancionatorio previsto en la Ley 1437 de 2011.
DISPOSICIONES FINALES.
ARTÍCULO 37. AUTORIZACIÓN PARA EL AGOTAMIENTO DE EXISTENCIAS DE ETIQUETAS, USO DE ADHESIVOS Y ETIQUETA COMPLEMENTARIA. <Artículo corregido por el artículo 2 de la Resolución 254 de 2023. El nuevo texto es el siguiente:> Para el agotamiento de existencias de etiquetas, uso de adhesivos y etiqueta complementaria, se seguirán las siguientes reglas:
37.1. Los titulares del registro, permiso o notificación sanitaria de alimentos y bebidas envasados, que ya hayan implementado lo relacionado con el etiquetado frontal de advertencia (sello circular) y nutricional, y aquellos que continúen cumpliendo lo establecido en la Resolución 333 de 2011, podrán radicar solicitud de agotamiento de etiquetas por una sola vez ante el INVIMA hasta el 28 de febrero de 2023. El INVIMA definirá el plazo de agotamiento, sin superar el término establecido en el numeral 40.3 del artículo 40 del presente acto administrativo.
37.2. Los responsables de los alimentos envasados o empacados podrán hacer uso de adhesivos sobre la etiqueta, según lo establecido en el artículo 32, siempre y cuando los adhesivos cumplan exactamente con las disposiciones contenidas en el presente reglamento técnico. Esta alternativa no requerirá previa autorización por parte del INVIMA.
37.3. Para productos importados, siempre que se cuente con el Certificado de Inspección Sanitaria (CIS), emitido por parte del Invima o la autoridad competente, se permitirá el uso de un rótulo o etiqueta complementaria que contenga la información exigida en la presente resolución, la cual deberá ir adherida en lugar visible y su ajuste se podrá realizar antes, durante o después del proceso de nacionalización y antes de su comercialización.
37.4. Para el caso de los productos nacionales, se permitirá el uso de un rótulo o etiqueta complementaria que contenga únicamente la información nutricional exigida en la presente resolución, la cual deberá ir adherida en lugar visible, hasta el 15 de diciembre de 2023, sin autorización de Invima o hasta máximo, el 15 de junio de 2024, cuando se cuente con autorización de la misma entidad.
ARTÍCULO 38. REVISIÓN Y ACTUALIZACIÓN. Con el fin de mantener actualizadas las disposiciones del reglamento técnico que se establece con la presente resolución, el Ministerio Salud y Protección Social, de acuerdo con los avances científicos y tecnológicos nacionales e internacionales y las evidencias existentes, procederá a su revisión en un término no mayor a cinco (5) años, contados a partir de la fecha en vigencia, o antes, si se detecta que las causas que motivaron su expedición fueron modificadas o desaparecieron.
ARTÍCULO 39. NOTIFICACIÓN. El presente reglamento técnico será notificado a través del punto de contacto OTC (Obstáculos Técnicos al Comercio) del Ministerio de Comercio, Industria y Turismo, a los países integrantes de la Organización Mundial del Comercio (OMC).
ARTÍCULO 40. TRANSITORIEDAD. <Artículo corregido por el artículo 3 de la Resolución 254 de 2023. El nuevo texto es el siguiente:> La implementación de los requisitos técnicos de etiquetado nutricional y frontal seguirá las siguientes reglas:
40.1. Las disposiciones modificatorias establecidas en este acto administrativo, así como los demás requisitos descritos en el reglamento técnico de etiqueta nutricional y frontal, serán implementados dentro de los seis (6) meses siguientes a la fecha de la publicación de este acto en el Diario Oficial, periodo en el cual, los titulares de registros, permisos y notificaciones sanitarias, productores, importadores y comercializadores de los alimentos envasados para consumo humano y los demás sectores obligados al cumplimiento de lo aquí dispuesto, deberán adaptar sus procesos y productos de acuerdo con las condiciones establecidas en el reglamento técnico.
40.2. Los fabricantes que deseen ajustar el etiquetado nutricional y frontal de advertencia en las etiquetas antes de los seis (6) meses previstos en el inciso anterior, podrán hacerlo, dando total cumplimiento a lo exigido en este acto administrativo.
40.3. A partir del 15 de junio de 2024, los alimentos envasados y empacados que no cumplan con el etiquetado nutricional y frontal de advertencia establecido en el reglamento técnico deberán ser retirados del mercado por el productor o comercializador, independientemente de la fecha de fabricación, comercialización o empacado del alimento.
40.4. Para el caso de los envases retornables se otorgará un tiempo de cinco (5) años contados a partir de la fecha de publicación del presente acto administrativo en el Diario Oficial, para el cumplimiento de las condiciones previstas en el reglamento técnico. Sin embargo, a partir del 16 de junio de 2023, el sello frontal de advertencia se deberá colocar en la tapa para los envases retornables que no puedan etiquetarse en la cara frontal, o con un adhesivo o en el envase secundario.
40.5. Los emprendedores deberán cumplir los requisitos establecidos en la reglamentación técnica de etiquetado nutricional y frontal de advertencia, en el tiempo estipulado en la reglamentación que se expida, conforme con el artículo 7o de la Ley 2254 de 2022.
PUBLÍQUESE, NOTIFÍQUESE Y CÚMPLASE.
Dada en Bogotá, D. C., a 16 de junio de 2021.
El Ministro de Salud y Protección Social,
Fernando Ruiz Gómez